Цель. В статье рассмотрены вопросы этиопатогенеза, клиники и диагностики альвеолярного легочного протеиноза на примере клинического случая пациента с альвеолярным протеинозом.
Особенности клинического случая. Представленный случай идиопатического альвеолярного протеиноза (АП) характеризуется минимальными клиническими проявлениями заболевания при выраженных изменениях в легочной ткани по данным лучевых методов исследования органов грудной клетки. Диагноз АП был подтвержден морфологически.
Заключение. Альвеолярный протеиноз представляет собой редкое заболевание легких интерстициальной природы, в основе которого лежит нарушение клиренса сурфактанта с накоплением в просвете альвеол патологического белково-липидного вещества. Выделяют три основных формы АП: врожденный, приобретенный (идиопатический) и вторичный АП. Основа диагностики АП – характерные изменения при мультиспиральной компьютерной томографии органов грудной клетки и данные морфологического исследования.
Введение. Альвеолярный протеиноз (АП) представляет собой редкое заболевание легких интерстициальной природы, в основе которого лежит нарушение клиренса сурфактанта с накоплением в просвете альвеол патологического белково-липидного вещества [1]. Впервые заболевание было описано в 1958 году Rosen et al. [2], и к настоящему времени в литературе опубликовано около 500 клинических случаев [3]. Встречается, как правило, в возрасте 30-50 лет, преимущественно у мужчин.
Этиология и патогенез АП. Выделяют три основных формы АП: врожденный, приобретенный (идиопатический) и вторичный АП [3]. Врожденный АП обусловлен мутациями генов, кодирующих синтез белков сурфактанта типа В или С, либо ?с-цепи рецептора к гранулоцитарно-макрофагальному колониестимулирующему фактору (ГМ-КСФ). Патогенез идиопатического АП связывают с наличием аутоиммунных антител к ГМ-КСФ, приводящих к повреждению либо функциональной недостаточности этого белка [4]; такая форма наиболее часто встречается у лиц молодого возраста. Вторичный АП развивается в результате воздействия этиологических факторов, приводящих к снижению числа и дисфункции альвеолярных макрофагов. К числу этиологических факторов вторичного АП относят: вирусные и бактериальные инфекции (микобактерии, грибы, пневмоцисты), контакт с аэрополлютантами (кремний, алюминий, пластмассы, тяжелые металлы), иммуносупрессивные состояния, в том числе лекарственно-обусловленные, гемобластозы (лейкозы, лимфомы) и др. [5].
Общепринятая концепция патогенеза АП заключается в следующем: под влиянием этиологических факторов в альвеолах появляется воспалительный экссудат, что приводит к активации альвеолярных макрофагов (АМ) и лимфатической системы с целью удаления белково-липидной фракции из альвеол. Одновременно происходит выработка альвеолоцитами II типа избыточного количества измененного сурфактанта, не обладающего поверхностно-активными свойствами. Большие количества сурфактанта поглощаются АМ, что вызывает развитие в них дегенеративных изменений и приводит к снижению их функциональной активности. Нагруженные липидной фракцией макрофаги - один из основных морфологических признаков АП. Вследствие указанных изменений в альвеолах происходит дальнейшее прогрессивное накопление белково-липидного вещества в их просвете. В свою очередь, это усиливает компенсаторную гиперфункцию альвеолоцитов II типа и приводит к еще большей продукции сурфактанта и усугубляет нарушение функции АМ. Таким образом происходит формирование патогенетического «порочного круга».
Патоморфологическая картина АП характеризуется следующими особенностями: преимущественное поражение базальных и задних отделов легких (плевра и средостение интактны); наличие на поверхности легких серовато-белых бугорков в виде зерен; наличие в альвеолах и бронхиолах больших количеств эозинофильного гранулярного ШИК-положительного белково-липидного вещества; наличие в просвете альвеол нагруженных липидной фракцией АМ («пенистые» макрофаги); гиперплазия и гипертрофия альвеолоцитов II типа [6].
Помимо вышеизложенного, одним из универсальных механизмов патогенеза всех форм АП является нарушение функции АМ, обусловленное дефицитом ключевого регулятора липидного обмена – рецептором активации пролиферации пероксисом ? (peroxisome proliferator-activated receptor ?) [7]. Недостаточность этого фактора приводит к повышению уровня холестерина и его метаболитов в бронхоальвеолярном лаваже [8]. Недостаточность этого фактора может быть скорректирована с помощью заместительной терапии ГМ-КСФ [9]. Интересно, что протеинозоподобные патогистологические изменения в ткани легких наблюдаются у мышей, в геноме которых отсутствует ген, кодирующий синтез ГМ-КСФ [9, 10], а ингаляционное введение этого биологически активного вещества уменьшает выраженность подобных изменений [11, 12].
При АП наибольшим изменениям подвергается система сурфактанта. Сурфактант продуцируется альвеолоцитами II типа и состоит на 90% из липидной фракции и на 10% - из белковой, а также из небольшого количества углеводных цепей. Приблизительно 80-90% липидной фракции представлено фосфолипидами, оставшуюся часть составляют холестерин, триацилглицерол и ненасыщенные жирные кислоты [13]. Изучение процессов синтеза, репарации и биодеградации сурфактанта в настоящее время является одним из приоритетных направлений пульмонологических исследований. Описано два основных пути катаболизма сурфактанта [14]: первый заключается в реализации полного цикла рециркуляции веществ, образующих сурфактант, в альвеолоцитах II типа; второй подразумевает обеспечение клиренса сурфактанта с помощью его фагоцитоза и биодеградации в альвеолярных макрофагах [15]. Регуляция этих путей осуществляется путем взаимодействия целого ряда цитокинов, в первую очередь, ГМ-КСФ, реализующего свои эффекты через соответствующие рецепторы [16]. Любые нарушения синтеза либо реализации действия этого фактора неизбежно приводят к развитию патологического процесса в альвеолах, обусловленного накоплением избыточного количества липидно-белковой субстанции, что лежит в основе развития и прогрессирования врожденного и идиопатического АП. Также немаловажную роль играют интерлейкины (ИЛ) (ИЛ-10, ИЛ-12 и ИЛ-18)[17], которые регулируют синтез ГМ-КСФ, механизмы локального фагоцитоза и синтеза антител и интерферонов [18]. Так формируется вторичный иммунологический дефект, обуславливающий присоединение вторичной инфекции и ухудшение прогноза у больных АП, что требует проведения первичной и вторичной антибактериальной и противовирусной профилактики.
Диагностика АП включает в себя сбор клинико-анамнестических данных (выявление семейного анамнеза, оценка синдрома дыхательной недостаточности), проведение компьютерной томографии органов грудной клетки и морфологическую верификацию [19]. Основным методом лечения АП в настоящее время является бронхоальвеолярный лаваж (БАЛ) [20]. Показано, что применение этого метода для симптоматической терапии АП дает стойкую ремиссию заболевания длительностью от нескольких месяцев до нескольких лет [20]. Также патогенетически обоснованными методиками терапии являются введение ГМ-КСФ (как парентерально, так и ингаляционно) и экстракорпоральные методы лечения, среди которых ведущее место занимают плазмаферез и применение мембранных оксигенаторов [21].
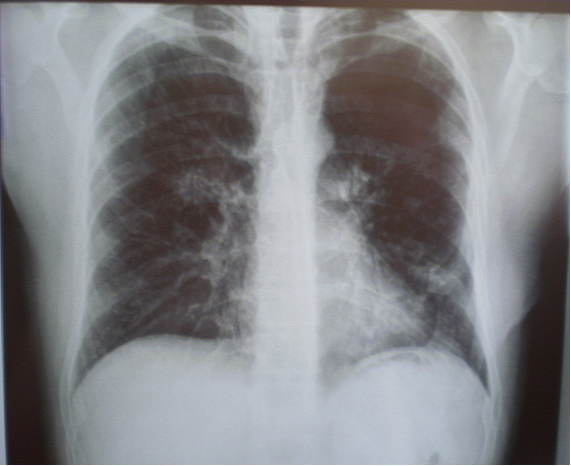
Клинический случай. Больной П., 32 лет, поступил в пульмонологическое отделение НУЗ «ЦКБ №1 ОАО «РЖД» в связи с выявлением при диспансерном обследовании изменений на флюорограмме в виде усиления и деформации легочного рисунка в прикорневых областях обоих легких. Амбулаторно была проведена рентгенография органов грудной клетки, на которой вышеуказанные изменения были подтверждены (рис. 1). Для дообследования и верификации диагноза направлен в стационар.
Рисунок 1. Рентгенограмма органов грудной клетки больного П.: легочный рисунок диффузно усилен и деформирован на всем протяжении за счет интерстициального компонента
При поступлении жалоб не предъявляет. Ранее проблем со стороны органов дыхания не отмечал. Около двух месяцев назад выявлены вышеописанные изменения на рентгенограмме ОГК, требующие уточнения характера интерстициальных изменений в легких. Клинически значимых хронических заболеваний в анамнезе нет. Наследственность не отягощена. Аллергологический анамнез: пыльца растений – риноконъюнктивит (симптоматическая терапия препаратами антигистаминового ряда). Проживает в районе с повышенной задымленностью (рядом с домом – промышленное предприятие). Профессия – помощник машиниста локомотива, проходил ежегодное медицинское освидетельствование. В анамнезе – табакокурение с индексом 15 пачка-лет. В детском и юношеском возрасте занимался легкой атлетикой, имеет спортивный разряд.
В объективном статусе клинически значимых отклонений от нормы не выявлено.
Общеклинические анализы крови и мочи, биохимический анализ крови – без патологии. По лабораторным данным отмечается повышение IgE до 189,6 Ме/мл (N до 100). АТ к ВИЧ (ИФА) - не обнаружены. HBs-антиген, анти-НСV (ИФА) - не обнаружены. RW- отр.
Исследование газового состава артериальной крови: рН – 7,394, рСО2 – 40,8 мм. рт. ст., рО2 – 86,3 мм. рт. ст. SaO2 – 98% (при дыхании атмосферным воздухом).
Цитологическое исследование биоптата слизистой бронхов: группы клеток цилиндрического эпителия, небольшое число лейкоцитов, макрофаги, слизь.
Данные инструментальных исследований: ЭКГ, ФВД – значимых отклонений от референсных значений не выявлено.
Фибробронхоскопия: картина двухстороннего эндобронхита.
Компьютерная томография органов грудной полости: на серии компьютерных томограмм получены изображения легких и средостения в аксиальной плоскости на уровне вдоха по стандартному протоколу. Легкие обычных размеров и формы, с дополнительной долей непарной вены в правом легком. Легочный рисунок резко деформирован по мелко- и среднепетлистому типу в прикорневых отделах с обеих сторон. Также отмечаются участки и зоны деформации легочного рисунка по мелко- и среднепетлистому типу и по типу «матового стекла» в плащевых отделах легких с обеих сторон – симптом «географической карты». Во всех отделах определяются множественные плевральные сращения. Корни легких структурны, с наличием множественных бронхопульмональных лимфатических узлов (0,2-0,5 см в диаметре) в структуре. Стенки трахеи и бронхов умеренно уплотнены, с наличием мелких бронхоэктазов в задне-базальных отделах слева. Сердце умеренно увеличено в размерах, преимущественно за счет левых отделов. Жидкости в плевральных полостях не обнаружено (рис. 2).
Рисунок 2а. Компьютерная томограмма органов грудной клетки: изменения легочного рисунка по типу «матового стекла». Множественные плевральные сращения
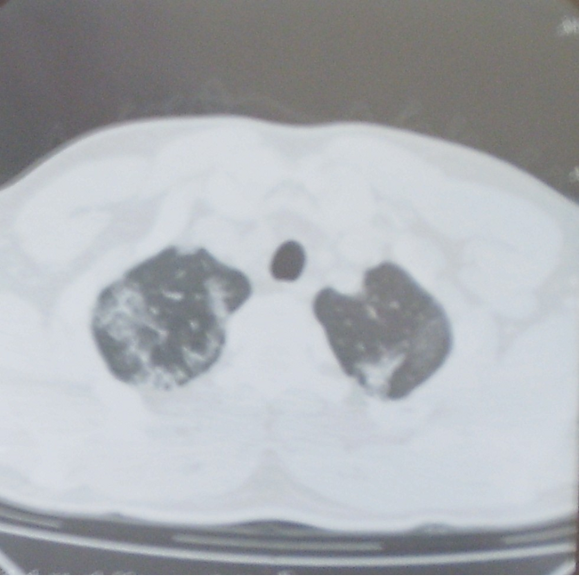
Рисунок 2б. Компьютерная томограмма органов грудной клетки: изменения легочного рисунка по типу «матового стекла». Множественные плевральные сращения
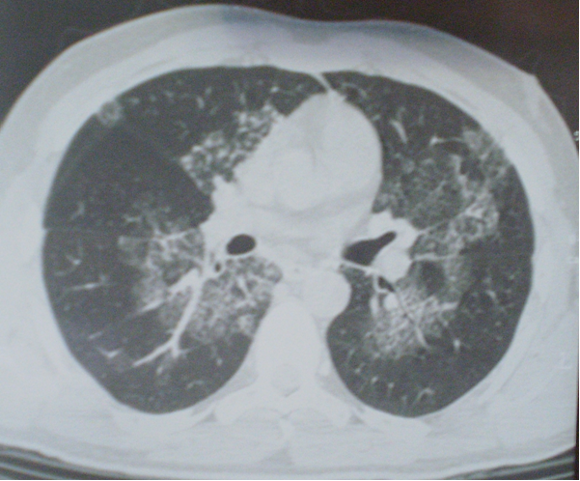
С целью морфологической верификации диагноза больному была произведена операция в объеме торакоскопии плевральной полости слева, миниторакотомии слева, краевой аппаратной резекции язычкового сегмента левого легкого.
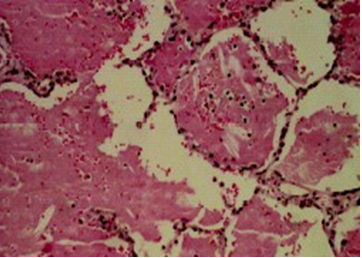
Проведено морфологическое исследование: в микропрепаратах ткань легкого, гистоархитектоника которой не нарушена. В просвете некоторых альвеол определяется эозинофильное гранулярное вещество с кристаллоидными включениями. Альвеолоциты II типа гиперплазированы. В отдельных полях зрения обнаруживается повышенное количество альвеолярных макрофагов. Часто обнаруживаются очаговые лимфоцитарные инфильтраты. Заключение: гистологическая картина характерна для легочного альвеолярного протеиноза (рис. 3).
Рисунок 3. Гиперплазия стенки бронхиол и скопление аморфного эозинофильного материала в просвете альвеол, мелкоточечные геморрагии (гематоксилин-эозин, х200)
Заключение. Таким образом, на основании данных компьютерной томографии органов грудной полости и данных морфологического исследования был сформулирован клинический диагноз: идиопатический легочный альвеолярный протеиноз, состояние после торакоскопии плевральной полости слева, миниторакотомии слева, краевой аппаратной резекции язычкового сегмента левого легкого. ДН 0 ст.
Представленный клинический случай характеризуется следующими особенностями:
- отсутствие клинических проявлений заболевания (одышка, кашель, и др.);
- нетипичная для АП локализация поражения: по данным КТ ОГК отмечается поражение не только задне-базальных, но и верхних отделов легких (рис 2). Помимо этого, визуализируется поражение плевры в виде множественных плевральных сращений, что не характерно для АП.
- отсутствие показаний для проведения бронхоальвеолярного лаважа (в первую очередь, признаков прогрессирующей дыхательной недостаточности) обусловило дальнейшую тактику ведения пациента: рекомендовано наблюдение в динамике и проведение БАЛ при ухудшении клинического статуса.
Список литературы:
1. Kitamura T., Tanaka N., Watanabe J., Uchida K., Kanegasaki S., Yamada Y., Nakata K. Idiopathic pulmonary alveolar proteinosis as an autoimmune disease with neutralizing antibody against granulocyte/macrophage colony-stimulating factor. J Exp Med 1999; 190:875-80.
2. Rosen S.H., Castleman B., Liebow A.A. Название статьи? N Engl J Med 1958; 258: 1123-42.
3. Ceruti M., Rodi G., Stella G.M., Adami A., Bolongaro A., Baritussio A., Pozzi E., Luisetti M. Successful whole lung lavage in pulmonary alveolar proteinosis secondary to lysinuric protein intolerance: a case report. Orphanet Journal of Rare Diseases 2007;1750-7.
4. Seymour J.F., Presneill J.J. Pulmonary alveolar proteinosis (progress in the first 44 years). Am J Respir Crit Care Med 2002; 166:215-35.
5. Xie L., Zhao T., Wang Q., Chen L., Li A., Wang D., Qi F., Liu Y. Secondary pulmonary alveolar proteinosis associated with myelodisplastic syndrome. Clin Med J 2007; 120 (12):1114-6.
6. Vourlekis J.S., Greene K.E. Pulmonary alveolar proteinosis. Interstitial Lung Disease 2006; 865-76.
7. Bonfield T.L., Farver C.F., Barna B.P., Malur A., Abraham S., Raychaudhuri B., Kavuru M.S., Thomassen M.J. Peroxisome proliferator-activated receptor-gamma is deficient in alveolar macrophages from patients with alveolar proteinosis. Am J Respir Cell Mol Biol 2003; 29: 677-82.
8. Meaney S., Bonfield T.L., Hansson M., Babiker A., Kavuru M.S., Thomassen M.J. Serum cholestenoic acid as a potential marker of pulmonary cholesterol homeostasis: increased levels in patients with pulmonary alveolar proteinosis. J Lipid Res 2004; 45:2354-60.
9. Stanley E., Lieschke G.J., Grail D. еt al.. Granulocyte/macrophage colony-stimulating factor-deficient mice show no major perturbation of hematopoesis but develop a characteristic pulmonary pathology. Proc Natl Acad Sci USA 1994; 91:5592-6.
10. Dranoff G., Crawford A.D., Sadelain M. еt al. Involvement of granulocyte-macrophage colony-stimulating factor in pulmonary homeostasis. Science 1994; 264:713-6.
11. Huffman J.A., Hull W.M. Dranoff G., Mulligan R.C., Whitsett J.A. Pulmonary epithelial cell expression of GM-CSF corrects the alveolar proteinosis in GM-CSF-deficient mice. J Clin Invest 1996; 97:649-55.
12. Reed J.A., Ikegami M., Cianciolo E.R. еt al. Aerosolized GM-CSF ameliorates pulmonary alveolar proteinosis in GM-CSF-deficient mice. Am J Physiol 1999; 276: L556-L63.
13. Akino T. Lipid components of the surfactant system. In: Pulmonary surfactant. B. Robertson, L.M.G. van Golde and J.J. Batenburg, editors. 1992. Elsevier, Amsterdam. 19-31.
14. Hawgood S., Poutain F.R. The pulmonary collectins and surfactant metabolism. Annu Rev Physiol 2001; 63:495-519.
15. Trapnell B.C., Whitsett J.A., Nakata K. Pulmonary alveolar proteinosis. N Engl J Med 2003; 349:2527-39.
16. Trapnell B.C., Whitsett J.A. GM-CSF regulates pulmonary surfactant homeostasis and alveolar macrophage-mediated innate host defense. Annu Rev Physiol 2002; 64:775-802.
17. Yoshida M., Whitsett J.A. Interaction between pulmonary surfactant and alveolar macrophages in pathogenesis of lung disease. Cell Mol Biol 2004; 50:OL639 – OL648.
18. Wylam M.E., Ten R., Prakash U.B., Nadrous H.F., Clawson M.L., Anderson P.M. Aerosol
granulocyte-macrophage colony-stimulating factor for pulmonary alveolar proteinosis. Eur Respir J 2006; 27:585-93.
19. Shah P.L., Hansell D., Lawson P.R. et al. Pulmonary alveolar proteinosis: clinical aspects and current concept on pathogenesis. Thorax 2000; 55:67-77.
20. Dexter M.E., Cosgrove G.P., Douglas I.S. Managing a rare condition presenting with intractable hypoxemic respiratory failure. Chest 2007; 131:320-7.
21. Spock A. Long-term survival of pediatric patients with pulmonary alveolar proteinosis treated with lung lavage. Eur Respir J 2005; 25:1127.