Заболевания, ассоциированные с повышенной желудочной кислотопродукцией, являются на сегодняшний день важной и нерешенной социально-экономической проблемой. В США ежегодно регистрируются 90000 случаев заболевания язвенной болезнью (ЯБ), 3000 больных умирают от данной патологии. В целом 15% американцев имеют диагноз ЯБ, у 5% это ЯБ желудка, у 95% – двенадцатиперстной кишки (http://emedicine.medscape.com/article/368602-overview). Ежегодное число госпитализаций по поводу острого кровотечения как осложнения ЯБ составляет 103 случая на 100000 населения [37, 45].
Распространенность ЯБ в Российской Федерации в 2003 году составила 1268,9 случаев на 100000 населения. Наибольший показатель зарегистрирован в Приволжском и Центральном федеральном округах – 1423,4 и 1364,9 на 100000 населения соответственно. Согласно отчетам Министерства здравоохранения, в 2003 году в России на диспансерном учете находилось 3 миллиона больных. Язвенный дефект в 4 раза чаще локализовался в двенадцатиперстной кишке, чем в желудке. Смертность от болезней органов пищеварения, включая ЯБ, составила 183,4 на 100000 населения. За последующие годы уровень заболеваемости существенно не изменился [4].
По информации американской ассоциации гастроэнтерологов прямые и непрямые затраты на лечение ЯБ составляют около 25 млрд. долларов в год [21]. Единые данные, касающиеся экономических затрат при лечении ЯБ в России, к сожалению, отсутствуют.
Заболеваемость гастроэзофагеальной рефлюксной болезнью (ГЭРБ) в последние годы увеличивается. Распространенность изжоги и эрозивного эзофагита максимальна в США и странах Западной Европы (около 20 % населения) и минимальна в Сингапуре (2%), Китае (2,5 %) и Корее (3,5 %); Россия занимает промежуточное положение (около 10 %) [5, 16]. Имеются данные, что в США в 2005 году, по сравнению с 1998 годом, количество рефлюкс-эзофагитов увеличилось на 94%, а на лечение ГЭРБ ежегодно расходуется около 19 миллионов долларов [39, 40].
ГЭРБ – частая причина болей в грудной клетке. Экономическое значение этой проблемы в США было рассмотрено еще в 1989 году, когда на начальное лечение каждого пациента с болью неустановленной этиологии ежегодно расходовалось около 3500 долларов. За последующие 16 лет эти затраты значительно увеличились [20].
Экономические потери, связанные с лечением ГЭРБ, должны оцениваться комплексно, так как данный вид патологии кроме значительного снижения качества жизни пациентов, вероятно, вызывает развитие или является причиной обострений бронхиальной астмы, ряда отоларингологических, стоматологических заболеваний [25, 38].
Применение нестероидных противовоспалительных препаратов (НПВС) ассоциировано с высоким риском возникновения клинически значимых патологических состояний в верхних отделах пищеварительного тракта, включая симптоматические язвы желудка и двенадцатиперстной кишки, а также их возможные осложнения (кровотечения, перфорации). В США ежегодно на приобретение НПВС по назначению врачей расходуется около 5 миллионов долларов, при этом затраты на лечение нежелательных явлений, связанных с приемом препаратов данной фармакологической группы, превышают 2 миллиона долларов [29]. Уточненные данные для РФ не приводятся.
Таким образом, наблюдается широкая распространенность патологии органов пищеварительного тракта, ассоциированной с высокой интенсивностью кислотопродукции в желудке и часто возникающей на фоне применения нестероидных противовоспалительных препаратов. Для терапии таких состояний наиболее эффективной и безопасной группой препаратов являются ингибиторы протонной помпы (ИПП). До недавнего времени широко применялись блокаторы гистаминовых Н2-рецепторов, но сегодня значение данной группы снижается из-за многочисленности случаев резистентности и низкой клинической эффективности при ГЭРБ [34].
Особенности российского фармацевтического рынка препаратов–ИПП обусловлены значительными межрегиональными различиями оптовых цен, большими различиями розничных цен в аптеках и, в первую очередь, наличием большого количества более дешевых генериков при отсутствии доказательной базы их терапевтической эквивалентности. Проводимые в обязательном порядке исследования биоэквивалентности у здоровых добровольцев не гарантируют ее у пациентов с кислотозависимой патологией слизистых оболочек пищеварительного тракта, у которых биодоступность ИПП может значительно снижаться [8]. При этом применение фармакоэкономического анализа для генериков на основе моделей, создаваемых на основе результатов рандомизированных исследований оригинальных препаратов, представляется не совсем корректным. Так, например, проведенные в Италии и Великобритании фармакоэкономические исследования убедительно свидетельствуют о преимуществе назначения при ГЭРБ эзомепразола (Нексиум®) 40 мг/сут., по сравнению с омепразолом 20 мг/сут.; эзомепразола 20 мг «по требованию», по сравнению с омепразолом 20 мг/сут.; эзомепразола 20 мг/сут., по сравнению с лансопразолом 30 мг/сут. [10, 31, 42]. Учитывая цены на оригинальные и генерические препараты, а также стоимость медицинских услуг по ОМС в РФ, фармакоэкономические преимущества Нексиума® в сравниваемых парах перестают быть очевидными. Описываемым зарубежными авторами преимуществам применения эзомепразола сопутствует высокая оценка, которую дают этому препарату пациенты (Таблица 1).
Таблица 1. Оценка пациентами преимуществ лечения эзомепразолом, по сравнению с другими ингибиторами протонной помпы, – результаты обсервационного мультицентрового исследования (n=4929) [26]
![Оценка пациентами преимуществ лечения эзомепразолом, по сравнению с другими ингибиторами протонной помпы, – результаты обсервационного мультицентрового исследования (n=4929) [26]](/files/articles/gepatologiya/serebrova_table_1.png)
Мы провели ряд сравнительных исследований, направленных на уточнение фармакоэкономической эффективности Нексиума®, по сравнению с другими ИПП, при его назначении больным с заболеваниями, ассоциированными с высокой интенсивностью желудочной кислотопродукции. Фармакоэкономические модели для расчета эффективности затрат на лечение кислотозависимой патологии пищеварительного тракта создавались с учетом
- оптовых и розничных цен на сравниваемые препараты;
- стоимости курсовых доз препаратов;
- действующих Стандартов амбулаторно-поликлинической помощи при болезнях органов пищеварения [9];
- тарифов обязательного медицинского страхования (ОМС) г. Москвы на оказание медицинской помощи, актуальных на февраль 2010 года. Так как доля ОМС в общих затратах на медицинскую помощь составляет примерно 1/3, рассчитанные по тарифам ОМС затраты умножались на поправочный коэффициент 3 [6]. Стоимость медицинских услуг при первичном, повторных (с частотой, рекомендуемой «Стандартами») обращениях и при коррекции терапии в случае ее неэффективности рассчитывалась раздельно.
Если в качестве показателя эффективности применялась доля времени, в течение которого желудочный рН>4 (показатель, коррелирующий с клинической эффективностью), коэффициент стоимость / эффективность (CER – cost-effectivenes ratio) рассчитывался по формуле
CER = C / Е, где
С – стоимость курсовой дозы;
Е – эффективность: доля времени (% от 24ч), в течение которой сохранялся уровень желудочного рН>4.
Если в качестве показателя эффективности использовалась доля пациентов, у которых за определенный промежуток времени наблюдалось заживление дефектов слизистых оболочек пищеварительного тракта, то коэффициент CER рассчитывался по формуле
CER = (С + 3 * (С1 + С2 + nC3)) / Е, где
С – стоимость курсовой дозы;
С1 – затраты на медицинские услуги при первичном обращении;
С2 – затраты на медицинские услуги при повторных обращениях;
С3 – затраты на медицинские услуги при коррекции терапии;
n – доля пациентов, нуждающихся в коррекции терапии;
Е – эффективность: количество пациентов (абсолютное значение или доля (в %) от общего количества), у которых наблюдалось заживление дефектов слизистых оболочек. Относительное значение может быть использовано при одинаковом количестве больных в сравниваемых группах или при пересчете затрат на лечение одинакового числа пациентов.
Учитывая наличие на российском фармацевтическом рынке большого количества препаратов-генериков ИПП, резко различающихся по уровням цен и спроса, мы включили в исследование препараты производителей, вошедших в рейтинг ТОП-50 фармацевтических компаний-лидеров по уровню продаж (данные за сентябрь 2009 года).
Средние оптовые цены рассчитывались на основании ежедневно обновляемой базы данных сайта «Фарманалитик» (http://fbr.info/db/pr/) по прайс-листам фармацевтических компаний-производителей и дистрибьюторов. Средние розничные цены рассчитывались на основании цен, представленных на сайте «Aptekamos.ru» (http://aptekamos.ru). Учитывая значительные различия розничных цен в разных аптеках и регионах, мы учитывали цены в аптеках, входящих в состав 10 аптечных сетей, в которых сравниваемые препараты в г.Москве были представлены не менее чем в 9 аптеках. Средние оптовые и розничные цены рассчитаны для 02.02.2010г. и пересчитаны на 14 таблеток/капсул.
Таблица 2. Средние оптовые, розничные цены (Mean ± SE) и розничная наценка для препаратов-ингибиторов протонной помпы (14 таблеток или капсул)
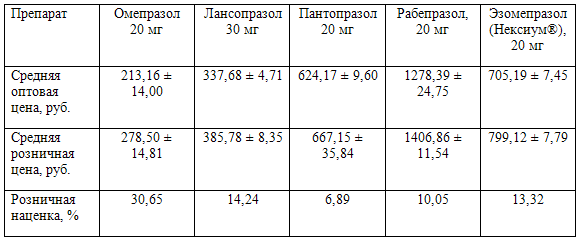
Практическое применение фармакоэкономических методов должно быть осторожным. Не секрет, что при расчете коэффициента CER, зависящего от соотношения значений числителя и знаменателя, может быть продемонстрировано экономическое преимущество препарата с более низкой клинической эффективностью и значительно более дешевого. Например, при использовании фармакоэкономической модели на основе мультицентрового рандомизированного в параллельных группах исследования, проведенного в 163 клинических центрах в США с участием 2425 пациентов с эрозивным эзофагитом, было показано, что через 4 недели приема Нексиума® 40 мг/сут. и омепразола 20 мг/сут. заживление эрозий наблюдалось в 81,7% и 68,7% случаев соответственно. Даже учитывая двойные (по сравнению с омепразолом) дозы и более высокую стоимость Нексиума® значения CER (по оптовым ценам) для эзомепразола и омепразола составили соответственно 128,64 и 118,12 (8,9?%). Нетрудно посчитать, таким образом, что при снижении коэффициента стоимость / эффективность на 1% за счет снижения затрат на используемый препарат качество контроля ГЭРБ снизится минимум на 1,46% (при условии, что клиническая эффективность дешевых генериков омепразола будет соответствовать таковой у препарата, использованного в США при проведении мультицентрового исследования) [35].
Сравнительный фармакоэкономический анализ использования эзомепразола и пантопразола, основанный на моделях, где в качестве суррогатного маркера эффективности использовалась доля времени, в течение которого желудочный рН>4, продемонстрировано преимущество эзомепразола.
При создании фармакоэкономических моделей использовались результаты многоцентровых рандомизированных исследований.
В рандомизированном слепом двукратно перекрестном исследовании, в котором участвовали 30 здоровых добровольцев, было показано, что через 5 дней приема эзомепразола и пантопразола по 40 мг/сут. время, в течение которого желудочный рН>4 на фоне применения эзомепразола составляет 21,4ч (89,67%), а на фоне приема пантопразола 16,8ч (70,00%). Доля ночного времени с рН>4 для эзомепразола составляет 85,4%, а для пантопразола 63,6%. В соответствии с оптовыми (опт) и розничными (розн) ценами для эзомепразола CERопт = 7,86; CERрозн = 8,91; для пантопразола CERопт = 8,92; CERрозн = 9,53. При оценке эффективности затрат на купирование ночной кислотопродукции для эзомепразола CERопт = 8,26; CERрозн = 9,36; для пантопразола CERопт = 9,81; CERрозн = 10,49 [33].
В открытом мультицентровом сравнительном трехкратно перекрестном исследовании, проведенном у 90 пациентов, длительно получавших нестероидные противовоспалительные препараты, проведено сравнение продолжительности антисекреторного эффекта эквивалентных доз (40 мг) эзомепразола и пантопразола. Через 5 дней приема сравниваемых препаратов доля времени, в течение которого рН > 4, было равно соответственно 74,2%, 60,8% (р<0,001). CERопт = 6,79 и CERрозн = 7,69 для эзомепразола; CERопт = 7,33 и CERрозн = 7,84 для пантопразола. Таким образом, более низкая клиническая эффективность пантопразола в отношении желудочной кислотопродукции сочетается с более низкой фармакоэкономической эффективностью, по сравнению с эзомепразолом, назначаемым в эквивалентных дозах [23].
В рандомизированном исследовании изучалось влияние эзомепразола и пантопразола, назначаемых по 20, 40 и 80 мг/сут. в течение 5 дней, на желудочный рН у больных с симптомами ГЭРБ. Препараты в указанных дозах назначались 35-36 пациентам [12]. Результаты данного исследования представлены в таблице 3.
Таблица 3. Влияние пятидневного применения эзомепразола и пантопразола в дозах 20, 40 или 80 мг на внутрижелудочный рН
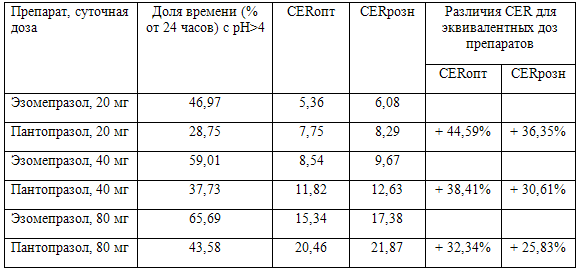
В рандомизированном сравнительном исследовании влияния 40 мг/сут. эзомепразола и пантопразола на заживление слизистой оболочки при эрозивном эзофагите (EXPO) показано, что через 4 недели лечения эпителизация произошла при применении эзомепразола и пантопразола соответственно у 81% и 75% больных (p<0,001). Для сравниваемых препаратов CERопт составляет соответственно 135,50 и 144,00, а CERрозн – соответственно 140,15 и 146,29. Через 8 недель лечения доля пациентов с зажившими эрозиями составила соответственно 96% и 92% (p<0,001). CERопт составляет для эзомепразола и пантопразола соответственно 141,82 и 142,00, CERрозн – соответственно 149,64 и 145,74. Более высокие через 8 недель значения CER для эзомепразола, по сравнению с пантопразолом (инверсия фармакоэкономического преимущества), объясняются эпителизацией эрозий практически у всех пациентов в обеих группах, более высокими розничными ценами на обладающий бoльшим спросом эзомепразол и могут быть снижены выбором более дешевых аптек [27].
В том же исследовании при сравнении влияния длительной поддерживающей терапии эзомепразолом 20 мг/сут. (n=2766) и пантопразолом 20 мг/сут.(n=1389) на состояние слизистой оболочки пищевода у больных с гастроэзофагеальной рефлюксной болезнью после документально подтвержденного заживления эрозий оказалось, что через 6 мес. доля больных с ремиссией заболевания была более высокой при применении эзомепразола (87,0%), чем при применении пантопразола (74,9%; р<0,0001). При этом доля пациентов, у которых отсутствовали симптомы ГЭРБ средней и тяжелой степени, были также достоверно более высокими в группе, где применяли эзомепразол, по сравнению с группой, где принимали пантопразол (соответственно 92,2% и 88,5%; р<0,001). CERопт для эзомепразола и пантопразола равен соответственно 172,05 и 189,68, CERрозн – соответственно 186,17 и 197,18, что свидетельствует о фармакоэкономическом преимуществе применении эзомепразола (CER ниже на 8,2% по оптовым и на 4,0% по розничным ценам) [28].
В перекрестном исследовании, в котором участвовали 23 здоровых добровольца, сравнивали влияние эзомепразола и рабепразола, назначаемых по 20 мг/сут., на желудочную кислотопродукцию. На пятый день приема препаратов доля времени, в течение которого желудочный рН>4, на фоне приема эзомепразола и рабепразола составлял соответственно 61% и 45,1%, p = 0,005. CER для эзомепразола составила 23,12 (оптовые цены) и 26,20 (розничные цены), а для рабепразола 28,35 (оптовые цены) и 31,19 (розничные цены) [44].
По данным проспективного рандомизированного исследования, в котором проводилась сравнительная оценка эффективности рабепразола (20 мг/сут.) и эзомепразола (20 и 40 мг/сут.) у больных с эндоскопически негативной ГЭРБ (n=1392), было показано, что влияние этих ИПП на симптомы заболевания одинаково и не зависит от доз. Оценка симптомов проводилась ежедневно в течение недели и однократно через 4 недели после начала лечения [19]. Разница в затратах на 7-недельную терапию ИПП представлена в таблице 4.
Таблица 4. Разница в затратах при применении рабепразола и эзомепразола в 4-недельной терапии ГЭРБ (n=1392)
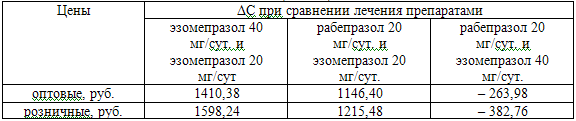
Расчеты проводились по формуле
dC = C1 – C2, где
dС – разница в затратах, C1 и С2 – затраты на лечение при использовании соответственно рабепразола и эзомепразола.
Отрицательные значения dС при сравнении результатов применения рабепразола 20 мг/сут. и эзомепразола 40 мг/сут. свидетельствуют о более низкой экономической обоснованности применения эзомепразола по 40 мг в сутки для купирования симптомов ГЭРБ, принимая также во внимание не зависящую от дозы одинаковую клиническую эффективность указанных ингибиторов протонной помпы. Таким образом, назначение эзомепразола по 20 мг/сут. является эффективным, достаточным и фармакоэкономически обоснованным при проведении длительной поддерживающей терапии эндоскопически негативной ГЭРБ.
Проведенные А.В.Рудаковой фармакоэкономические моделирующие исследования на основе контролируемых клинических испытаний показали, что применение эзомепразола позволяет снизить стоимость лечения рефлюкс-эзофагита, по сравнению с рабепразолом, на 18-21%. При терапии "по требованию" ГЭРБ без эзофагита минимальная стоимость лечения также продемонстрирована для эзомепразола (экономия 3-17% средств). Автором сделан вывод, что использование у пациентов с ГЭРБ эзомепразола является экономически более оправданным, независимо от наличия или отсутствия эзофагита [7].
Метаанализ, проведенный по материалам Европейской исследовательской группы по H.pylori и Конгрессов Американской гастроэнтерологической ассоциации с 1996 по 2002г., показал идентичную эффективность всех ИПП в 7-14 дневной стандартной тройной терапии инфекции H.pylori [41]. Анализ минимизации затрат при использовании представленных на российском фармацевтическом рынке оригинальных ИПП показывает, что ?С на 7-дневную стандартную терапию рабепразолом и эзомепразолом составляет 573,20 руб. (оптовые цены) и 607,74 руб. (розничные цены), а на 14-дневную терапию она равна 1146,40 руб. (оптовые цены) и 1215,48 руб. (розничные цены). В расчетах не учитывалась стоимость медицинских услуг, одинаковая при использованных схемах лечения.
Метаанализ рандомизированных контролируемых исследований, в которых изучалась эффективность блокаторов Н2-гистаминовых рецепторов и ИПП в отношении симптомов и дефектов слизистой оболочки пищевода при ГЭРБ (эзофагите средней и тяжелой степени) показал, что ИПП обладают заживляющей активностью в 83,6% случаев, блок Н2-рецепторов – в 51,9% случаев [15]. Обсуждать фармакоэкономическую эффективность применения Н2-блокаторов, клиническая эффективность которых в отношении симптомов ГЭРБ низка, не вполне корректно. Однако, сравнение значений показателя «затраты / эффективность», рассчитываемого на 6-месячный курс терапии с учетом стоимости медицинских ресурсов и замены блокаторов Н2-рецепторов в случае их неэффективности на эзомепразол, показало увеличение эффективности затрат при использовании эзомепразола на 14,7%, по сравнению с ранитидином, и 13,8%, по сравнению с фамотидином. Коэффициент CER для эзомепразола, ранитидина и фамотидина равен соответственно 178,19; 204,38 и 202,78.
Наиболее грозным осложнением язвенной болезни является кровотечение, и его профилактике, методам предотвращения рецидивов и лечению уделяется много внимания с клинической и экономической точки зрения. Ежегодно в США на лечение кровотечений при язвенной болезни расходуется 2 миллиона долларов [24]. Аналогичные данные для РФ, к сожалению, не представлены. При лечении больных с гастродуоденальным кровотечением обычно применяют препараты, снижающие интенсивность желудочной кислотопродукции. Несмотря на то, что блокаторы гистаминовых Н2-рецепторов достаточно часто назначаются пациентам с гастроинтестинальным кровотечением, результаты мультицентрового рандомизированного исследования (n=1005), проведенного в Великобритании, а также данные метаанализа 27 рандомизированных контролируемых исследований (n=2500), свидетельствуют, что эффективность представителей данной фармакологической группы не превышает эффективности плацебо или эндоскопического гемостаза без последующей коррекции кислотообразования [17, 43].
В то же время внутривенные формы ингибиторов протонной помпы рассматриваются как высокоэффективные средства профилактики рецидивирующего кровотечения, а некоторые авторы считают эффективным и фармакоэкономически оправданным начало парентерального применения ИПП до гастроскопии при появлении клинических признаков кровотечения [11]. Тем не менее, фармакоэкономические данные нуждаются в переоценке в соответствии с действующими на территории РФ тарифами на медицинские услуги и цены на препараты.
Результаты международного клинического исследования (Идентификатор сайта ClinicalTrials.gov: NCT00251979) показали, что применяемый в высоких дозах эзомепразол для внутривенного введения эффективно предотвращает риск повторного кровотечения у больных с язвенной болезнью после эндоскопического гемостаза [13]. В исследовании сравнивалось влияние вводимого внутривенного эзомепразола (80 мг инфузионно в течение 30 минут, затем по 8 мг/ч в течение 71,5 ч) и плацебо на частоту развития повторного кровотечения у пациентов после гемостаза. В обеих группах с 4 по 30 сутки лечения пациенты получали эзомепразол перорально по 40 мг в день. На протяжении 30 дней лечения рецидивы кровотечения наблюдались у 7,7% больных, получавших эзомепразол парентерально, и у 13,6% пациентов, получавших плацебо. Соотношение коэффициентов стоимость (доллары США) – эффективность для основной и контрольной групп составило 1,064. Используя данное исследование при создании фармакоэкономической модели, следует учитывать, что включить в расчет стоимость всех медицинских ресурсов, которые могут потребоваться, не представляется возможным. Вариабельными факторами, которые могут прогрессивно увеличивать коэффициент стоимость / эффективность при неудовлетворительных результатах лечения, будут интенсивность кровотечения, объем кровопотери, метод остановки кровотечения (консервативный, эндоскопический, оперативный), стоимость средств для коррекции гиповолемии, инфузионно-трансфузионной, гемостатической терапии и т.д. Известно, что у 10-14% пациентов кровотечение заканчивается летальным исходом. Общая летальность при рецидиве острого язвенного гастродуоденального кровотечения составляет около 15%, а послеоперационная достигает 40-60% [2]. Согласно шкале оценки риска Rockall, вероятность повторного кровотечения в зависимости от возраста, основного диагноза, сопутствующих заболеваний, некоторых особенностей течения патологического процесса повышается до 41,8%, при этом смертность может достигать 41,1% [36].
Таким образом, формула расчета эффективности затрат должна включать, по меньшей мере, составляющую неэффективных затрат, связанных с 15%-ной летальностью при повторных кровотечениях.
СER = X + (C/E) = (EX + C)/E, где
Х – составляющая затрат, эффективность которых не рассматривается в связи со смертностью 15% при повторных кровотечениях;
С – затраты на лечение;
Е – эффективность: абсолютное или относительное (в %) количество больных, у которых рецидивов кровотечения не было. Относительное значение может быть использовано при одинаковом количестве больных в сравниваемых группах или при пересчете затрат на лечение одинакового числа пациентов.
При расчете затрат использованы тарифы ОМС на лечение кровотечения из желудочно-кишечного тракта (24 дня), на оказание неотложной помощи хирургического профиля (включена стоимость за 1 сутки – минимально возможное количество дней, когда требуется данный вид помощи), стоимость койко-дня в хирургическом стационаре, средние оптовые цены на пероральный и парентеральный нексиум (http://fbr.info/db/pr/).
В группах больных, где использовалось плацебо и применялся эзомепразол парентерально, значения коэффициента CER составили соответственно 346893,06 и 299861,28 (соотношение CER равно 1,157). Таким образом, применение парентерального эзомепразола у больных с гастродуоденальным кровотечением после эндоскопического гемостаза повышает эффективность затрат на профилактику рецидивов кровотечения на 15,7%.
В настоящее время широко распространенной практикой стало использование омепразола (Лосек®) для парентерального применения в качестве препарата для профилактики рецидивов гастродуоденального кровотечения, несмотря на отсутствие соответствующих показаний в утвержденной Инструкции. В отсутствие таких показаний и при дефиците данных рандомизированных исследований невозможно создание серьезной доказательной базы эффективности Лосека®. Тем не менее, представления о сравнительной клинической и фармакоэкономической эффективности инъекционных Лосека® и Нексиума® могут быть сформулированы на основании упомянутого выше исследования [13] и опубликованной работы Daneshmend T.K. с соавт. [18]. На фоне болюсного введения 80 мг омепразола с последующими повторными внутривенными, а затем пероральными введениями Лосека® рецидив кровотечения наблюдался в 18% случаев. Значения CER при использовании эзомепразола и омепразола составляют соответственно 299861,28 и 315336,73 (соотношение CER равно 1,052). Таким образом, констатируя широко используемое на практике, но необоснованное применение Лосека® для профилактики рецидивов кровотечения, мы утверждаем, что использование Нексиума®, по сравнению с Лосеком®, повышает эффективность затрат на 5,2%.
Результаты опубликованного J. P. Gisbert с соавт. [22] метаанализа исследований, в которых сравнивалась клиническая эффективность вводимых внутривенно болюсно ИПП и блокаторов гистаминовых Н2-рецепторов при лечении язвенных кровотечений, свидетельствуют, что при использовании ИПП, по сравнению с Н2-блокаторами, наблюдается снижение частоты рецидивов кровотечения в 2 раза, хирургических вмешательств в 1,33 раз, частоты смертельных исходов в 1,38 раз (Табл. 5).
Таблица 5. Результаты применения инъекционных ИПП и блокаторов гистаминовых Н2-рецепторов при язвенном кровотечении по данным метаанализа J. P. Gisbert с соавт. [22]
![Результаты применения инъекционных ИПП и блокаторов гистаминовых Н2-рецепторов при язвенном кровотечении по данным метаанализа J. P. Gisbert с соавт. [22]](/files/articles/gepatologiya/serebrova_table_5.png)
При использовании данных этого метаанализа для формирования фармакоэкономической модели коэффициент CER для инъекционных эзомепразола, ранитидина и фамотидина составляет соответственно 300978,79; 340002,07 и 339863,25. Таким образом, инъекционный эзомепразол (Нексиум®), кроме значительно более высокой, по сравнению с Н2-блокаторами, клинической эффективности при лечении язвенных кровотечений, имеет также более высокие фармакоэкономические показатели: эффективность затрат при применении Нексиума® увеличивается на 12,97%, по сравнению с ранитидином, и на 12,92%, по сравнению с фамотидином.
В целом, следует отметить, что применение Н2-блокаторов для профилактики рецидивов кровотечения должно быть крайне осторожным. Вероятный конфликт механизма действия этих препаратов с доминирующим у больного гормональным (гастринергическим) или нейро-рефлекторным (обусловленным преобладающей активностью n.vagus) механизмом стимуляции кислотопродукции, быстрое развитие толерантности к Н2-блокаторам могут иметь фатальные последствия [1, 3, 14, 32]. Для Н2-блокаторов характерен феномен «рекошета» в виде резкого усиления кислотопродукции после отмены препарата. Ранитидин и фамотидин могут вызвать психические расстройства, что создает дополнительную опасность для пациентов в тяжелом состоянии. Кроме того, Н2-блокаторы обладают сравнительно низкой клинической эффективностью при гастроэзофагеальной рефлюксной болезни, а также при профилактике и лечении повреждений слизистых оболочек при длительном применении нестероидных противовоспалительных препаратов [30, 34].
Мы рассмотрели фармакоэкономические аспекты применения препарата Нексиум® у больных с кислотозависимой патологией пищевода, желудка и двенадцатиперстной кишки. Несмотря на сравнительно высокие цены на Нексиум®, особенно по сравнению с препаратами-генериками ИПП, применение эзомепразола является эффективным и экономически обоснованным при ГЭРБ, язвенной болезни и связанном с ней гастродуоденальном кровотечении.
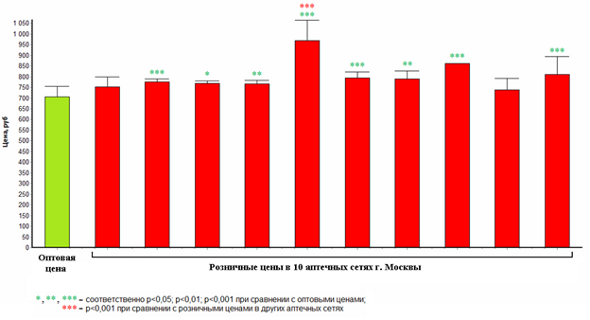
Рис. 1. Оптовые и розничные цены (Mean ± SE) препарата Нексиум® 20 мг (14 таблеток)
Литература
01. Блинков И.Л., Селина Е.В., Карелина Е.А., Кукес В.Г. Способ лечения язвенной болезни. Авт. Свидет. № 1362477 (Бюл. О.И. 48, 1987).
02. Гостищев В.К., Евсеев М.А. Острые гастродуоденальные кровотечения: от стратегических концепций к лечебной тактике. - М.: Анта-Эко, 2005. - 352 с
03. Журавлева М.В. Клиническая фармакология блокаторов Н2-гистаминовых рецепторов. – Дисс. докт. мед. наук. – Москва, 2000. – С.337.
04. Здравоохранение в России. 2005: Стат. сб. М: Росстат. – 2006. – 390 с.
05. Исаков В.А. Эпидемиология ГЭРБ: Восток и Запад // Экспериментальная клиническая гастроэнтерология. – 2004. – №5 (Спецвыпуск). – С. 2-6.
06. Клинико-экономический анализ // Под ред. П.А.Воробьева. М.: Ньюдиамед, 2004. – 404с.
07. Рудакова А.В. Фармакоэкономические аспекты применения рабепразола и эзомепразола у пациентов с гастроэзофагеальной рефлюксной болезнью. Consilium medicum/ приложение/ гастроэнтерология. – 2006. – №1. – C.13-17.
08. Сереброва С.Ю., Стародубцев А.К., Писарев В.В., Кондратенко С.Н. и др. Фармакокинетика, продолжительность антисекреторного эффекта омепразола и эзомепразола, вероятные причины их изменений при язвенной болезни двенадцатиперстной кишки // Экспериментальная и клиническая гастроэнтерология. - 2009. - N 4 . - С. 86-92.
09. Стандарты амбулаторно-поликлинической помощи при болезнях органов пищеварения. Сайт Межрегиональной общественной организации «Общество фармакоэкономических исследований»
10. A study to assess the effectiveness of maintenance treatment with esomeprazole 20mg od in patients with reflux disease previously maintained with lansoprazole 30mg od - A 3 month, randomised, double blind, double dummy, multicentre study- (30/20 Study). SUMMARY. AstraZeneca Clinical Trials web site
11. Al–Sabah S., Barkun A.N., Herba K., Adam V. et al. Cost-Effectiveness of Proton-Pump Inhibition Before Endoscopy in Upper Gastrointestinal Bleeding // Clin Gastroenterol Hepatol. – 2008. – Vol.6. – P.418– 425.
12. An Open, Single-Centre, Randomized, 6-way Crossover, Dose-Response Comparative Study of Esomeprazole 20, 40 and 80 mg and Pantoprazole 20, 40 and 80 mg regarding 24-hour Intragastric pH following 5 Days Repeated Oral Dose Administration in Patients with Symptoms of Gastroesophageal Reflux Disease. Synopsis of Clinical Study Report. AstraZeneca Clinical Trials web site
13. Barkun A., Adam V., Sung J., Kuipers E. et The cost-effectiveness of high-dose intravenous esomeprazole in peptic ulcer bleeding – a US cost perspective // Am J Gastroenterol – 2008. – Vol.103(suppl.1):S48 and ACG PUB CEA US Costs Poster Barkun et al. 2008.pdf
14. Barkun A., Bardou M., Marshall J.K. Consensus recommendations for managing patients with nonvariceal upper gastrointestinal bleeding // Ann Intern Med 2003; 139:843-857.
15. Chiba N., De Gara C.J., Wilkinson J.M., Hunt R.H. Speed of healing and symptom relief in grade II to IV gastroesophageal reflux disease: a meta-analysis // Gastroenterol 1997; 112: 1798-1810.
16. Cho Y.S., Choi M.G., Jeong J.J. Prevalence and clinical spectrum of gastroesophageal reflux: a population-based study in Asan-si, Korea // Am. J. Gastroenterol. – 2005. – Vol. 100. – №4. – P. 747-753.
17. Collins R., Langman M.: Treatment with histamine H2 antagonists in acute upper gastrointestinal hemorrhage. Implications of randomized trials // N Engl J Med. – 1985. – Vol.313. – P.660-666.
18. Daneshmend T.K., Hawkey C.J., Langman M.J., Logan R.F. et al. Omeprazole versus placebo for acute upper gastrointestinal bleeding: randomised double blind controlled trial // BMJ. – 1992. – Vol.304(6820). – P.143-147.
19. Eggleston A., Katelaris P.H., Nandurkar S., Thorpe P. et al. Clinical trial: the treatment of gastro-oesophageal reflux disease in primary care--prospective randomized comparison of rabeprazole 20 mg with esomeprazole 20 and 40 mg // Aliment Pharmacol Ther. – 2009. – Vol.29(9). – P.967-978.
20. Flook N., Unge P., Agreus L., Karlson B.W. et al. Approach to managing undiagnosed chest pain. Could gastroesophageal reflux disease be the cause? // Canadian Family Physician. – 2007. – Vol. 53. – P. 261-266.
21. Gilbert D.A., Silberstain F.E. Acute upper gastrointestinal bleeding // Gastroenterologic endoscopy. – 2000. – Vol. 1. – P. 284-299.
22. Gisbert J. P., Gonzalez L., Calvet X., Roque M., Gabriel R et al. Proton pump inhibitors versus H2-antagonists: a meta-analysis of their efficacy in treating bleeding peptic ulcer // Aliment Pharmacol Ther. 2001 Jul;15(7):917-26.
23. Goldstein J.L., Miner JR P. B., Schlesinger P. K., Liu S. et al. Intragastric acid control in non-steroidal anti-inflammatory drug users: comparison of esomeprazole, lansoprazole and pantoprazole // Alimentary Pharmacology & Therapeutics. – 2006. –Vol. 23(8). – P.1189-1196.
24. Gralnek I.M., Barkun A.N., Bardou M. Management of Acute Bleeding from a Peptic Ulcer // N Engl J Med. – 2008. – Vol.359. – P.928937.
25. Havemann B.D., Henderson C.A., El-Serag H.B. The association between gastro-oesophageal reflux disease and asthma: a systematic review // Gut – 2007. – Vol. 56. – P. 1654–1664.
26. Hoogendoorn R.J., Groeneveld L., Kwee J.A. Patient satisfaction with switching to esomeprazole from existing proton pump inhibitor therapy for gastro-oesophageal reflux disease: an observational, multicentre study // Clin Drug Investig. –2009. – Vol.29(12). – P.803-810.
27. Labenz J., Armstrong D., Lauritsen K., Katelaris P. et al. A randomized comparative study of esomeprazole 40 mg versus pantoprazole 40 mg for healing erosive oesophagitis: the EXPO study // Aliment Pharmacol Ther. – 2005. – Vol.21(6). – P.739-746.
28. Labenz J., Armstrong D., Lauritsen K., Katelaris P. et al. Esomeprazole 20 mg vs. pantoprazole 20 mg for maintenance therapy of healed erosive oesophagitis: results from the EXPO study1 // Aliment Pharmacol Ther. – 2005. – Vol.22(5). – P.803-811.
29. Laine L. Approaches to nonsteroidal anti-in?ammatory drug use in the high risk patient. Gastroenterology. – 2001. – Vol.120. – P.594–606
30. Lam NP, Le PD, Crawford SY, Patel S. National survey of stress ulcer prophylaxis // Crit Care Med. 1999;27:98-103.
31. Lucioni C., Mazzi S., Rossi C. Proton pump inhibitors in acute treatment of reflux oesophagitis : a cost-effectiveness analysis // Clin Drug Investig. – 2005. – Vol.25(5). – P.325-336.
32. Merki H.S., Wilder-Smith C.H. Do continuous infusions of omeprazole and ranitidine retain their effect with prolonged dosing? // Gastroenterology 1994; 106:60-644.
33. Miehlke S., Madisch A., Kirsch C., Lindner F. et al. Intragastric acidity during treatment with esomeprazole 40 mg twice daily or pantoprazole 40 mg twice daily – a randomized, two-way crossover study // Aliment Pharmacol Ther. – 2005. – Vol.21. – P. 963–967.
34. Modlin I.M., Sachs G. Acid related deseases: biology and treatment. – Schnetztor – Verlag GmbH D – Konstanz, 1998. – P. 197 - 241.
35. Richter J.E., Kahrilas P.J., Johanson J., Maton P. Efficacy and safety of esomeprazole compared with omeprazole in GERD patients with erosive esophagitis: a randomized controlled trial // The American Journal of Gastroenterology. – 2001. – Vol. 96. – P.656–665.
36. Rockall T.A., Logan R.F., Devlin H.B. et al. Risk assessment after acute upper gastrointestinal haemorrhage // Gut. – 1996. – Vol.38. – P.316-321.
37. Schwesinger W.H. Operations for peptic ulcer disease: a paradigm lost // J.Gastrointest. Surg. – 2001. – Vol. 5. – №4. – Р. 438-443.
38. Szarka L.A., Devault K.R., Murray J.A. Diagnosing Gastroesophageal Reflux Disease // Mayo Clin. Proc. – 2001. – Vol. 76. – P.97-101.
39. Tessier D.J. Medical, Surgical, and Endoscopic Management of Gastroesophageal Reflux Disease // The Permanente Journal. – 2009. – Vol. 13. – №1. – Р. 30-36.
40. U.S. Census Bureau, Population Division, Annual Estimates of the Population for the United States, Regions, and Divisions and U.S. Census Bureau, Current Population Reports < http://www.census.gov/popest/estimates.html>.
41. Vergara M., Vallve M., Gisbert J.P., Calvet X. Meta-analysis: comparative efficacy of different proton-pump inhibitors in triple therapy for Helicobacter pylori eradication // Aliment Pharmacol Ther. – 2003. – Vol.18(6). – P.647-654.
42. Wahlqvist P., Junghard O., Higgins A. Green J. Cost Effectiveness of Esomeprazole Compared with Omeprazole in the Acute Treatment of Patients with Reflux Oesophagitis in the UK // PharmacoEconomics. – 2002. – Vol.20(4). – P.279-287.
43. Walt R.P., Cottrell J., Mann S.G., Freemantle N.P., Langman M.J.S. Continuous intravenous famotidine for haemorrhage from peptic ulcer // Lancet. – 1992. –Vol.340. – P.1058-1062.
44. Wilder-Smith C.H., Rohss K., Nilsson-Pieschl C., et al.. Esomeprazole 40 mg provides improved intragastric acid control as compared with lansoprazole 30 mg and rabeprazole 20 mg in healthy volunteers // Digestion. – 2003. – Vol.68. – P.184–188.
45. Zittel T.T. Surgical managemant of peptic ulcer disease today – indication, technique and outcome // Langenbeck’s Arch. Surg. – 2000. – Vol. 385. – P. 84-96.