–Π–Β–Μ―¨ –Ψ–±–Ζ–Ψ―Ä–Α. –ü―Ä–Ψ–Α–Ϋ–Α–Μ–Η–Ζ–Η―Ä–Ψ–≤–Α―²―¨ –¥–Α–Ϋ–Ϋ―΄–Β –Μ–Η―²–Β―Ä–Α―²―É―Ä―΄, –Ω–Ψ―¹–≤―è―â–Β–Ϋ–Ϋ―΄–Β –Η–Ζ―É―΅–Β–Ϋ–Η―é –Φ–Ψ–Μ–Β–Κ―É–Μ―è―Ä–Ϋ―΄―Ö –Ψ―¹–Ϋ–Ψ–≤ –Ω–Α―²–Ψ–≥–Β–Ϋ–Β–Ζ–Α –Η –Ω–Ψ–Η―¹–Κ―É –Ϋ–Ψ–≤―΄―Ö –Ω–Β―Ä―¹–Ω–Β–Κ―²–Η–≤–Ϋ―΄―Ö –Φ–Η―à–Β–Ϋ–Β–Ι –≤ –Μ–Β―΅–Β–Ϋ–Η–Η –≤–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Ψ–Ι –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η–Η.
–†–Β–Ζ―É–Μ―¨―²–Α―²―΄ –Ω–Ψ―¹–Μ–Β–¥–Ϋ–Η―Ö ―Ä–Α–±–Ψ―². –Γ―É–Φ–Φ–Η―Ä–Ψ–≤–Α–Ϋ―΄ ―¹–Ψ–≤―Ä–Β–Φ–Β–Ϋ–Ϋ―΄–Β –Ϋ–Α―É―΅–Ϋ―΄–Β –¥–Α–Ϋ–Ϋ―΄–Β 26 –Μ–Η―²–Β―Ä–Α―²―É―Ä–Ϋ―΄―Ö –Η―¹―²–Ψ―΅–Ϋ–Η–Κ–Ψ–≤, –Ω―Ä–Β–Η–Φ―É―â–Β―¹―²–≤–Β–Ϋ–Ϋ–Ψ –Ζ–Α―Ä―É–±–Β–Ε–Ϋ―΄―Ö –Α–≤―²–Ψ―Ä–Ψ–≤. –£–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Α―è –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Α―è –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η―è (–£–€–î) βÄ™ –Ψ―¹–Ϋ–Ψ–≤–Ϋ–Α―è –Ω―Ä–Η―΅–Η–Ϋ–Α –Ϋ–Β–Ψ–±―Ä–Α―²–Η–Φ–Ψ–Ι ―¹–Μ–Β–Ω–Ψ―²―΄ ―É –Ω–Ψ–Ε–Η–Μ―΄―Ö –Μ―é–¥–Β–Ι –≤ ―Ä–Α–Ζ–≤–Η―²―΄―Ö ―¹―²―Ä–Α–Ϋ–Α―Ö. –ü–Ψ –¥–Α–Ϋ–Ϋ―΄–Φ –£―¹–Β–Φ–Η―Ä–Ϋ–Ψ–Ι –Ψ―Ä–≥–Α–Ϋ–Η–Ζ–Α―Ü–Η–Η –Ζ–¥―Ä–Α–≤–Ψ–Ψ―Ö―Ä–Α–Ϋ–Β–Ϋ–Η―è, ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²―¨ –¥–Α–Ϋ–Ϋ–Ψ–Ι –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Η ―¹–Ψ―¹―²–Α–≤–Μ―è–Β―² 300 ―΅–Β–Μ–Ψ–≤–Β–Κ –Ϋ–Α 100 ―²―΄―¹―è―΅ –Ϋ–Α―¹–Β–Μ–Β–Ϋ–Η―è, 25-30 –Φ–Μ–Ϋ. ―΅–Β–Μ–Ψ–≤–Β–Κ –≤ –Φ–Η―Ä–Β ―¹―²―Ä–Α–¥–Α–Β―² –£–€–î. –£ ―¹–≤―è–Ζ–Η ―¹ ―Ä–Ψ―¹―²–Ψ–Φ ―¹―Ä–Β–¥–Η –Ϋ–Α―¹–Β–Μ–Β–Ϋ–Η―è –¥–Ψ–Μ–Η –Μ–Η―Ü –Ω–Ψ–Ε–Η–Μ–Ψ–≥–Ψ –≤–Ψ–Ζ―Ä–Α―¹―²–Α –Η ¬Ϊ–Ψ–Φ–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η–Β–Φ¬Μ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è, –Ω―Ä–Ψ–±–Μ–Β–Φ–Α –£–€–î ―¹―²–Α–Ϋ–Ψ–≤–Η―²―¹―è –≤―¹–Β –±–Ψ–Μ–Β–Β –Α–Κ―²―É–Α–Μ―¨–Ϋ–Ψ–Ι, ―΅―²–Ψ ―è–≤–Μ―è–Β―²―¹―è –Φ–Ψ―â–Ϋ―΄–Φ ―¹―²–Η–Φ―É–Μ–Ψ–Φ –¥–Μ―è –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Η―è –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Ι, –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Ϋ―΄―Ö –Ϋ–Α ―Ä–Α–Ζ―Ä–Α–±–Ψ―²–Κ―É –Ϋ–Ψ–≤―΄―Ö –Ω–Β―Ä―¹–Ω–Β–Κ―²–Η–≤–Ϋ―΄―Ö –Ω–Ψ–¥―Ö–Ψ–¥–Ψ–≤ –Κ –Μ–Β―΅–Β–Ϋ–Η―é –£–€–î. –ù–Α―Ä―è–¥―É ―¹ ―Ä–Α–Ζ–≤–Η―²–Η–Β–Φ –Η ―¹–Ψ–≤–Β―Ä―à–Β–Ϋ―¹―²–≤–Ψ–≤–Α–Ϋ–Η–Β–Φ ―É–Ε–Β ―¹―É―â–Β―¹―²–≤―É―é―â–Η―Ö –Φ–Β―²–Ψ–¥–Ψ–≤ –Μ–Β―΅–Β–Ϋ–Η―è (–Η–Ϋ―²―Ä–Α–≤–Η―²―Ä–Β–Α–Μ―¨–Ϋ–Α―è –Α–Ϋ―²–Η-VEGF ―²–Β―Ä–Α–Ω–Η―è, –Μ–Α–Ζ–Β―Ä–Ϋ–Α―è ―³–Ψ―²–Ψ–Κ–Ψ–Α–≥―É–Μ―è―Ü–Η―è, ―³–Ψ―²–Ψ–¥–Η–Ϋ–Α–Φ–Η―΅–Β―¹–Κ–Α―è ―²–Β―Ä–Α–Ω–Η―è), –≤ –Κ–Α―΅–Β―¹―²–≤–Β –Φ–Η―à–Β–Ϋ–Β–Ι –Μ–Β–Κ–Α―Ä―¹―²–≤–Β–Ϋ–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Η –≤–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Ψ–Ι –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η–Η –Α–Κ―²–Η–≤–Ϋ–Ψ –Η―¹―¹–Μ–Β–¥―É―é―²―¹―è ―à–Α–Ω–Β―Ä–Ψ–Ϋ RPE65, ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä―΄ –Α–Κ―²–Η–≤–Α―Ü–Η–Η –Ω–Β―Ä–Ψ–Κ―¹–Η―¹–Ψ–Φ βÄ™ PPAR, –±–Β–Μ–Κ–Η ―³–Η–±―É–Μ–Η–Ϋ―΄ –Η ―ç―Ä–Η―²―Ä–Ψ–Ω–Ψ―ç―²–Η–Ϋ.
–½–Α–Κ–Μ―é―΅–Β–Ϋ–Η–Β. –‰–Ϋ―²–Β–Ϋ―¹–Η–≤–Ϋ–Ψ–Β –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –Φ–Ψ–Μ–Β–Κ―É–Μ―è―Ä–Ϋ―΄―Ö –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ–Ψ–≤ –±–Ψ–Μ–Β–Ζ–Ϋ–Η ―¹–Μ―É–Ε–Η―² –Ψ―¹–Ϋ–Ψ–≤–Ψ–Ι –¥–Μ―è ―¹–Ψ–≤–Β―Ä―à–Β–Ϋ―¹―²–≤–Ψ–≤–Α–Ϋ–Η―è –Μ–Β–Κ–Α―Ä―¹―²–≤–Β–Ϋ–Ϋ―΄―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤, ―²–Ψ―΅–Κ–Ψ–Ι –Ω―Ä–Η–Μ–Ψ–Ε–Β–Ϋ–Η―è –Κ–Ψ―²–Ψ―Ä―΄―Ö ―è–≤–Μ―è―é―²―¹―è –Η–Ζ–≤–Β―¹―²–Ϋ―΄–Β –Φ–Η―à–Β–Ϋ–Η –≤ –Μ–Β―΅–Β–Ϋ–Η–Η –£–€–î, –Η –Ψ―²–Κ―Ä―΄―²–Η―è –Ϋ–Ψ–≤―΄―Ö –Ω–Β―Ä―¹–Ω–Β–Κ―²–Η–≤–Ϋ―΄―Ö –Φ–Η―à–Β–Ϋ–Β–Ι, –≤–Ψ–Ζ–¥–Β–Ι―¹―²–≤―É―è –Ϋ–Α –Κ–Ψ―²–Ψ―Ä―΄–Β, –Φ–Ψ–Ε–Ϋ–Ψ –Ζ–Α–Φ–Β–¥–Μ–Η―²―¨ –Ω―Ä–Ψ–≥―Ä–Β―¹―¹–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β –Ω–Ψ―²–Β―Ä–Η –Ζ―Ä–Β–Ϋ–Η―è ―É –Ω–Ψ–Ε–Η–Μ―΄―Ö –Μ―é–¥–Β–Ι.
–£–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Α―è –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Α―è –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η―è (–£–€–î) βÄ™ –¥–Β–≥–Β–Ϋ–Β―Ä–Α―²–Η–≤–Ϋ–Ψ–Β, –Ω―Ä–Ψ–≥―Ä–Β―¹―¹–Η―Ä―É―é―â–Β–Β –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η–Β –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –Ψ–±–Μ–Α―¹―²–Η ―¹–Β―²―΅–Α―²–Κ–Η, ―è–≤–Μ―è―é―â–Β–Β―¹―è –≤–Β–¥―É―â–Β–Ι –Ω―Ä–Η―΅–Η–Ϋ–Ψ–Ι –Ω–Ψ―²–Β―Ä–Η ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ζ―Ä–Β–Ϋ–Η―è ―É –Ω–Ψ–Ε–Η–Μ―΄―Ö –Μ―é–¥–Β–Ι –≤ ―Ä–Α–Ζ–≤–Η―²―΄―Ö ―¹―²―Ä–Α–Ϋ–Α―Ö [1]. –£ ―¹―²―Ä―É–Κ―²―É―Ä–Β ―¹–Μ–Α–±–Ψ–≤–Η–¥–Β–Ϋ–Η―è –£–€–î –Ζ–Α–Ϋ–Η–Φ–Α–Β―² –≤―²–Ψ―Ä–Ψ–Β –Φ–Β―¹―²–Ψ –Η, –Κ–Α–Κ –Ω―Ä–Α–≤–Η–Μ–Ψ, ―¹–Ψ–Ω―Ä–Ψ–≤–Ψ–Ε–¥–Α–Β―²―¹―è –¥–≤―É―¹―²–Ψ―Ä–Ψ–Ϋ–Ϋ–Η–Φ –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Β–Φ (–Ψ–±–Α –≥–Μ–Α–Ζ–Α –Ω–Ψ―Ä–Α–Ε–Α―é―²―¹―è –≤ 60% ―¹–Μ―É―΅–Α–Β–≤) [2]. –ü–Ψ –¥–Α–Ϋ–Ϋ―΄–Φ –£―¹–Β–Φ–Η―Ä–Ϋ–Ψ–Ι –Ψ―Ä–≥–Α–Ϋ–Η–Ζ–Α―Ü–Η–Η –Ζ–¥―Ä–Α–≤–Ψ–Ψ―Ö―Ä–Α–Ϋ–Β–Ϋ–Η―è, ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²―¨ –¥–Α–Ϋ–Ϋ–Ψ–Ι –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Η ―¹–Ψ―¹―²–Α–≤–Μ―è–Β―² 300 ―΅–Β–Μ–Ψ–≤–Β–Κ –Ϋ–Α 100 ―²―΄―¹―è―΅ –Ϋ–Α―¹–Β–Μ–Β–Ϋ–Η―è, 25-30 –Φ–Μ–Ϋ. ―΅–Β–Μ–Ψ–≤–Β–Κ –≤ –Φ–Η―Ä–Β ―¹―²―Ä–Α–¥–Α–Β―² –£–€–î. –£ –≤–Ψ–Ζ―Ä–Α―¹―²–Β ―¹―²–Α―Ä―à–Β 40 –Μ–Β―² –Ζ–Α–±–Ψ–Μ–Β–≤–Α―é―² 25-40% –Ϋ–Α―¹–Β–Μ–Β–Ϋ–Η―è, ―¹―Ä–Β–¥–Η –Μ–Η―Ü ―¹―²–Α―Ä―à–Β 60 –Μ–Β―² –¥–Α–Ϋ–Ϋ–Α―è –Ω–Α―²–Ψ–Μ–Ψ–≥–Η―è –≤―΄―è–≤–Μ―è–Β―²―¹―è ―É 58% [3, 4]. –ü―Ä–Ψ–±–Μ–Β–Φ–Α ―Ä–Α–Ζ–≤–Η―²–Η―è –£–€–î ―¹―²–Α–Ϋ–Ψ–≤–Η―²―¹―è –≤―¹–Β –±–Ψ–Μ–Β–Β –Α–Κ―²―É–Α–Μ―¨–Ϋ–Ψ–Ι –≤ ―¹–≤―è–Ζ–Η ―¹ ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η–Β–Φ ―¹―Ä–Β–¥–Η –Ϋ–Α―¹–Β–Μ–Β–Ϋ–Η―è –¥–Ψ–Μ–Η –Μ―é–¥–Β–Ι –Ω–Ψ–Ε–Η–Μ–Ψ–≥–Ψ –≤–Ψ–Ζ―Ä–Α―¹―²–Α, –Α ―²–Α–Κ–Ε–Β –≤ ―¹–≤―è–Ζ–Η ―¹ ¬Ϊ–Ψ–Φ–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η–Β–Φ¬Μ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è, –Ϋ–Α–±–Μ―é–¥–Α―é―â–Β–Φ―¹―è –≤―¹–Μ–Β–¥―¹―²–≤–Η–Β –≤–Ϋ–Β–¥―Ä–Β–Ϋ–Η―è –≤ –Ϋ–Α―à―É –Ε–Η–Ζ–Ϋ―¨ –≤―¹–Β –Ϋ–Ψ–≤―΄―Ö –Η –Ϋ–Ψ–≤―΄―Ö –Κ–Ψ–Φ–Ω―¨―é―²–Β―Ä–Ϋ―΄―Ö –Η ―²–Β–Μ–Β–≤–Η–Ζ–Η–Ψ–Ϋ–Ϋ―΄―Ö ―²–Β―Ö–Ϋ–Ψ–Μ–Ψ–≥–Η–Ι.
–½–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η–Β –Ω―Ä–Β–¥―¹―²–Α–≤–Μ―è–Β―² ―¹–Ψ–±–Ψ–Ι ―Ö―Ä–Ψ–Ϋ–Η―΅–Β―¹–Κ–Η–Ι –¥–Η―¹―²―Ä–Ψ―³–Η―΅–Β―¹–Κ–Η–Ι –Ω―Ä–Ψ―Ü–Β―¹―¹ ―¹ –Ω―Ä–Β–Η–Φ―É―â–Β―¹―²–≤–Β–Ϋ–Ϋ―΄–Φ –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Β–Φ ―Ö–Ψ―Ä–Η–Ψ–Κ–Α–Ω–Η–Μ–Μ―è―Ä–Ϋ–Ψ–≥–Ψ ―¹–Μ–Ψ―è ―Ö–Ψ―Ä–Η–Ψ–Η–¥–Β–Η, –Φ–Β–Φ–±―Ä–Α–Ϋ―΄ –ë―Ä―É―Ö–Α –Η ―¹–Μ–Ψ―è –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è ―¹–Β―²―΅–Α―²–Κ–Η. –£―¹–Μ–Β–¥―¹―²–≤–Η–Β ―²–Β―¹–Ϋ–Ψ–≥–Ψ –≤–Ζ–Α–Η–Φ–Ψ–¥–Β–Ι―¹―²–≤–Η―è ―¹―²―Ä―É–Κ―²―É―Ä–Ϋ―΄―Ö ―ç–Μ–Β–Φ–Β–Ϋ―²–Ψ–≤ ―¹–Β―²―΅–Α―²–Κ–Η –≤ –Ω–Α―²–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Ι –Ω―Ä–Ψ―Ü–Β―¹―¹ –≤–Κ–Μ―é―΅–Α―é―²―¹―è ―³–Ψ―²–Ψ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ϋ―΄–Β –Κ–Μ–Β―²–Κ–Η, ―΅―²–Ψ, –≤ –Κ–Ψ–Ϋ–Β―΅–Ϋ–Ψ–Φ –Η―²–Ψ–≥–Β, ―è–≤–Μ―è–Β―²―¹―è –Ω―Ä–Η―΅–Η–Ϋ–Ψ–Ι ―¹–Ϋ–Η–Ε–Β–Ϋ–Η―è –Ψ―¹―²―Ä–Ψ―²―΄ ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ζ―Ä–Β–Ϋ–Η―è. –ö ―³–Α–Κ―²–Ψ―Ä–Α–Φ ―Ä–Η―¹–Κ–Α ―Ä–Α–Ζ–≤–Η―²–Η―è –£–€–î –Ψ―²–Ϋ–Ψ―¹―è―² –≤–Ψ–Ζ―Ä–Α―¹―², –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è ―¹–Β―Ä–¥–Β―΅–Ϋ–Ψ-―¹–Ψ―¹―É–¥–Η―¹―²–Ψ–Ι ―¹–Η―¹―²–Β–Φ―΄ (–Α―²–Β―Ä–Ψ―¹–Κ–Μ–Β―Ä–Ψ–Ζ –Η –Α―Ä―²–Β―Ä–Η–Α–Μ―¨–Ϋ–Α―è –≥–Η–Ω–Β―Ä―²–Β–Ϋ–Ζ–Η―è), –Κ―É―Ä–Β–Ϋ–Η–Β, –Η–Ζ–±―΄―²–Ψ―΅–Ϋ–Ψ–Β ―É–Μ―¨―²―Ä–Α―³–Η–Ψ–Μ–Β―²–Ψ–≤–Ψ–Β –Ψ–±–Μ―É―΅–Β–Ϋ–Η–Β, –Ϋ–Β―¹–±–Α–Μ–Α–Ϋ―¹–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–Β –Ω–Η―²–Α–Ϋ–Η–Β, ―¹–≤–Β―²–Μ―΄–Ι (–≥–Ψ–Μ―É–±–Ψ–Ι) ―Ü–≤–Β―² –≥–Μ–Α–Ζ [5]. –€―É―²–Α―Ü–Η–Η –Η –Ω–Ψ–Μ–Η–Φ–Ψ―Ä―³–Η–Ζ–Φ –≥–Β–Ϋ–Ψ–≤, –Κ–Ψ―²–Ψ―Ä―΄–Β –¥–Β―²–Β―Ä–Φ–Η–Ϋ–Η―Ä―É―é―² –±–Β–Μ–Κ–Η, ―É―΅–Α―¹―²–≤―É―é―â–Η–Β –≤ –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ–Ψ–Φ –Κ–Α―¹–Κ–Α–¥–Β, ―³–Α–Κ―²–Ψ―Ä―΄ –Κ–Ψ–Φ–Ω–Μ–Β–Φ–Β–Ϋ―²–Α –ù, CFB –Η –Γ2, –Α–Ω–Ψ–Μ–Η–Ω–Ψ–Ω―Ä–Ψ―²–Β–Η–Ϋ –ï, ―³–Η–±―É–Μ–Η–Ϋ―΄ 3 –Η 5, –Α―¹―¹–Ψ―Ü–Η–Η―Ä―É―é―²―¹―è ―¹ –Ω–Ψ–≤―΄―à–Β–Ϋ–Ϋ―΄–Φ ―Ä–Η―¹–Κ–Ψ–Φ ―Ä–Α–Ζ–≤–Η―²–Η―è –£–€–î –Η –±–Ψ–Μ–Β–Β ―²―è–Ε–Β–Μ―΄–Φ –Β–Β ―²–Β―΅–Β–Ϋ–Η–Β–Φ [6,7]. –û―¹–Ϋ–Ψ–≤–Ϋ―΄–Φ–Η –Ζ–≤–Β–Ϋ―¨―è–Φ–Η –Ω–Α―²–Ψ–≥–Β–Ϋ–Β–Ζ–Α –£–€–î ―è–≤–Μ―è―é―²―¹―è –Ω―Ä–Ψ―Ü–Β―¹―¹―΄ ―¹―²–Α―Ä–Β–Ϋ–Η―è –Κ–Μ–Β―²–Ψ–Κ ―¹–Β―²―΅–Α―²–Κ–Η, ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Α –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ü–Η–Κ–Μ–Α, –¥–Η―¹―²―Ä–Ψ―³–Η―΅–Β―¹–Κ–Η–Β –Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η―è –≤ –Φ–Β–Ε–Κ–Μ–Β―²–Ψ―΅–Ϋ–Ψ–Φ –Φ–Α―²―Ä–Η–Κ―¹–Β, ―Ä–Α–Ζ–≤–Η―²–Η–Β –Η–Φ–Φ―É–Ϋ–Ϋ–Ψ–≥–Ψ –≤–Ψ―¹–Ω–Α–Μ–Β–Ϋ–Η―è, –Ψ–Κ―¹–Η–¥–Α―²–Η–≤–Ϋ―΄–Ι ―¹―²―Ä–Β―¹―¹, –Ϋ–Α―Ä―É―à–Β–Ϋ–Η–Β –Μ–Η–Ω–Η–¥–Ϋ–Ψ–≥–Ψ –Ψ–±–Φ–Β–Ϋ–Α –Η –Ω–Α―²–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Ι –Α–Ϋ–≥–Η–Ψ–≥–Β–Ϋ–Β–Ζ (―Ä–Η―¹. 1) [8].
–ü–Ψ–Μ–Α–≥–Α―é―², ―΅―²–Ψ –Ψ―²–Ω―Ä–Α–≤–Ϋ–Ψ–Ι ―²–Ψ―΅–Κ–Ψ–Ι ―Ä–Α–Ζ–≤–Η―²–Η―è –£–€–î ―è–≤–Μ―è–Β―²―¹―è –Ϋ–Α–Κ–Ψ–Ω–Μ–Β–Ϋ–Η–Β –Μ–Η–Ω–Ψ―³―É―¹―Ü–Η–Ϋ–Ψ–≤―΄―Ö –≥―Ä–Α–Ϋ―É–Μ –≤ –Κ–Μ–Β―²–Κ–Α―Ö –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è, –Κ–Ψ―²–Ψ―Ä―΄–Β –≤―Ö–Ψ–¥―è―² –≤ ―¹–Ψ―¹―²–Α–≤ ―²–Α–Κ –Ϋ–Α–Ζ―΄–≤–Α–Β–Φ―΄―Ö –¥―Ä―É–Ζ. –ü―Ä–Η―΅–Β–Φ –Μ–Η–Ω–Ψ―³―É―¹―Ü–Η–Ϋ, –Κ–Α–Κ ―¹–≤–Β―²–Ψ–Ω–Ψ–≥–Μ–Ψ―â–Α―é―â–Η–Ι –Ω–Η–≥–Φ–Β–Ϋ―², ―¹–Ϋ–Α―΅–Α–Μ–Α –Φ–Ψ–Ε–Β―² –Η–≥―Ä–Α―²―¨ –Ω–Ψ–Μ–Ψ–Ε–Η―²–Β–Μ―¨–Ϋ―É―é ―Ä–Ψ–Μ―¨ –¥–Μ―è –Ζ–Α―â–Η―²―΄ ―¹–Β―²―΅–Α―²–Κ–Η –Ψ―² ―³–Ψ―²–Ψ–Ψ–Κ–Η―¹–Μ–Β–Ϋ–Η―è, –Ϋ–Ψ –≤ –≥–Μ–Α–Ζ―É –Ω–Ψ–Ε–Η–Μ–Ψ–≥–Ψ ―΅–Β–Μ–Ψ–≤–Β–Κ–Α –Κ–Ψ–Ϋ―Ü–Β–Ϋ―²―Ä–Α―Ü–Η―è –Μ–Η–Ω–Ψ―³―É―¹―Ü–Η–Ϋ–Α, –Ω–Ψ-–≤–Η–¥–Η–Φ–Ψ–Φ―É, –¥–Ψ―¹―²–Η–≥–Α–Β―² ―²–Ψ–Κ―¹–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –¥–Μ―è –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è ―É―Ä–Ψ–≤–Ϋ―è. –û―¹–Ϋ–Ψ–≤–Ϋ―΄–Φ –Κ–Ψ–Φ–Ω–Ψ–Ϋ–Β–Ϋ―²–Ψ–Φ –Μ–Η–Ω–Ψ―³―É―¹―Ü–Η–Ϋ–Ψ–≤―΄―Ö –≥―Ä–Α–Ϋ―É–Μ ―è–≤–Μ―è–Β―²―¹―è –≤–Β―â–Β―¹―²–≤–Ψ –ê2–ï. –£ ―²–Κ–Α–Ϋ―è―Ö –≥–Μ–Α–Ζ–Α –ê2–ï –Ψ–±―Ä–Α–Ζ―É–Β―²―¹―è –Η–Ζ-–Ζ–Α –Ϋ–Β―¹–Ω–Ψ―¹–Ψ–±–Ϋ–Ψ―¹―²–Η –Κ–Μ–Β―²–Ψ–Κ –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è –Ω–Ψ–Μ–Ϋ–Ψ―¹―²―¨―é –Ω–Β―Ä–Β–≤–Β―¹―²–Η –≤–Β―¹―¨ ―²―Ä–Α–Ϋ―¹-―Ä–Β―²–Η–Ϋ–Α–Μ―¨ –≤ 11-―Ü–Η―¹-―Ä–Β―²–Η–Ϋ–Α–Μ―¨. –î–Ψ–Ω–Ψ–Μ–Ϋ–Η―²–Β–Μ―¨–Ϋ―΄–Φ –Η―¹―²–Ψ―΅–Ϋ–Η–Κ–Ψ–Φ –ê2–ï ―è–≤–Μ―è―é―²―¹―è –¥–Η―¹–Κ–Η –Ϋ–Α―Ä―É–Ε–Ϋ―΄―Ö ―¹–Β–≥–Φ–Β–Ϋ―²–Ψ–≤ ―³–Ψ―²–Ψ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤, –Κ–Ψ―²–Ψ―Ä―΄–Β –Ω―É―²–Β–Φ ―³–Α–≥–Ψ―Ü–Η―²–Ψ–Ζ–Α –Ω–Ψ–Ω–Α–¥–Α―é―² –≤ –Κ–Μ–Β―²–Κ–Η –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è, –≥–¥–Β –ê2–ï –Ψ–±―Ä–Α–Ζ―É–Β―²―¹―è –≤ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Β –¥–Β–Ι―¹―²–≤–Η―è ―³–Β―Ä–Φ–Β–Ϋ―²–Ψ–≤ ―³–Α–≥–Ψ–Μ–Η–Ζ–Ψ―¹–Ψ–Φ. –ê2–ï –Η–Φ–Β–Β―² –Ω–Η―Ä–Η–¥–Η–Ϋ–Η–Β–≤―É―é –±–Η―¹―Ä–Β―²–Η–Ϋ–Ψ–Η–¥–Ϋ―É―é ―¹―²―Ä―É–Κ―²―É―Ä―É, –Κ–Ψ―²–Ψ―Ä–Α―è, –Ψ–¥–Ϋ–Α–Ε–¥―΄ –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–≤―à–Η―¹―¨, –Ϋ–Β –Φ–Ψ–Ε–Β―² –±―΄―²―¨ –Ω–Ψ–¥–≤–Β―Ä–Ε–Β–Ϋ–Α ―³–Β―Ä–Φ–Β–Ϋ―²–Α―²–Η–≤–Ϋ–Ψ–Φ―É ―Ä–Α–Ζ―Ä―É―à–Β–Ϋ–Η―é. –î–Ψ―¹―²–Η–≥–Ϋ―É–≤ –¥–Ψ―¹―²–Α―²–Ψ―΅–Ϋ–Ψ–Ι –Κ–Ψ–Ϋ―Ü–Β–Ϋ―²―Ä–Α―Ü–Η–Η, –ê2–ï –Φ–Ψ–Ε–Β―² –Ψ–Κ–Α–Ζ―΄–≤–Α―²―¨ –¥–Β―²–Β―Ä–≥–Β–Ϋ―²–Ψ–Ω–Ψ–¥–Ψ–±–Ϋ―΄–Β ―ç―³―³–Β–Κ―²―΄ –Ϋ–Α –Κ–Μ–Β―²–Ψ―΅–Ϋ―΄–Β –Φ–Β–Φ–±―Ä–Α–Ϋ―΄, –Ϋ–Α―Ä―É―à–Α―²―¨ ―³―É–Ϋ–Κ―Ü–Η–Ψ–Ϋ–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β –Μ–Η–Ζ–Ψ―¹–Ψ–Φ –Η –≤―΄―¹–≤–Ψ–±–Ψ–Ε–¥–Α―²―¨ –Ω―Ä–Ψ–Α–Ω–Ψ–Ω―²–Ψ–Ζ–Ϋ―΄–Β –±–Β–Μ–Κ–Η –Η–Ζ –Φ–Η―²–Ψ―Ö–Ψ–Ϋ–¥―Ä–Η–Ι. –ê2–ï –Ω–Ψ–≤―΄―à–Α–Β―² ―΅―É–≤―¹―²–≤–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ –Κ–Μ–Β―²–Ψ–Κ –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è –Κ –Ϋ–Α–Η–±–Ψ–Μ–Β–Β –Ψ–Ω–Α―¹–Ϋ–Ψ–Φ―É ―¹–Η–Ϋ–Β–Φ―É ―¹–≤–Β―²―É. –ü―Ä–Ψ–¥―É–Κ―²―΄ –Ψ–Κ–Η―¹–Μ–Β–Ϋ–Η―è –ê2–ï ―¹–Ω–Ψ―¹–Ψ–±–Ϋ―΄ ―Ä–Α–Ζ―Ä―É―à–Α―²―¨ –Φ–Α–Κ―Ä–Ψ–Φ–Ψ–Μ–Β–Κ―É–Μ―΄ –Κ–Μ–Β―²–Ψ–Κ. –£–¥–Ψ–±–Α–≤–Ψ–Κ, –ê2–ï –Φ–Ψ–Ε–Β―² –Η–Ϋ–≥–Η–±–Η―Ä–Ψ–≤–Α―²―¨ ―Ü–Η―²–Ψ―Ö―Ä–Ψ–Φ–Ψ–Κ―¹–Η–¥–Α–Ζ―É, ―΅―²–Ψ –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ –Ω―Ä–Β―Ä―΄–≤–Α–Ϋ–Η―é ―Ü–Β–Ω–Η –Ω–Β―Ä–Β–Ϋ–Ψ―¹–Α ―ç–Μ–Β–Κ―²―Ä–Ψ–Ϋ–Ψ–≤. –≠―²–Ψ –Ϋ–Β ―²–Ψ–Μ―¨–Κ–Ψ ―¹–Ϋ–Η–Ε–Α–Β―² ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ ―ç–Ϋ–Β―Ä–≥–Β―²–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Ψ–±–Φ–Β–Ϋ–Α –≤–Β―â–Β―¹―²–≤, –Ϋ–Ψ ―²–Α–Κ–Ε–Β –≤–Β–¥–Β―² –Κ ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η―é –Α–Κ―²–Η–≤–Ϋ―΄―Ö ―³–Ψ―Ä–Φ –Κ–Η―¹–Μ–Ψ―Ä–Ψ–¥–Α.
–î–Η―¹―²―Ä–Ψ―³–Η―΅–Β―¹–Κ–Η–Ι –Ω―Ä–Ψ―Ü–Β―¹―¹, –Μ–Β–Ε–Α―â–Η–Ι –≤ –Ψ―¹–Ϋ–Ψ–≤–Β ―Ä–Α–Ζ–≤–Η―²–Η―è –£–€–î, ―É―¹–Μ–Ψ–≤–Ϋ–Ψ –Φ–Ψ–Ε–Ϋ–Ψ ―Ä–Α–Ζ–¥–Β–Μ–Η―²―¨ –Ϋ–Α ―¹―²–Α–¥–Η–Η, ―΅―²–Ψ –Ω–Ψ–Ζ–≤–Ψ–Μ―è–Β―² –≤―΄–¥–Β–Μ–Η―²―¨ ―²―Ä–Η ―³–Ψ―Ä–Φ―΄ –£–€–î [9]:
I. –ù–Β―ç–Κ―¹―¹―É–¥–Α―²–Η–≤–Ϋ–Α―è (–Α―²―Ä–Ψ―³–Η―΅–Β―¹–Κ–Α―è) ―³–Ψ―Ä–Φ–Α. –û–Ϋ–Α ―¹–Ψ–Ω―Ä–Ψ–≤–Ψ–Ε–¥–Α–Β―²―¹―è ―Ä–Β―²–Η–Ϋ–Α–Μ―¨–Ϋ―΄–Φ–Η –¥–Β―³–Β–Κ―²–Α–Φ–Η –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è –Η –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η–Β–Φ –¥―Ä―É–Ζ. –î―Ä―É–Ζ―΄ ―è–≤–Μ―è―é―²―¹―è –Ω–Β―Ä–≤―΄–Φ–Η –Ω―Ä–Η–Ζ–Ϋ–Α–Κ–Α–Φ–Η –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è –Η –Μ–Ψ–Κ–Α–Μ–Η–Ζ―É―é―²―¹―è –Φ–Β–Ε–¥―É –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ―΄–Φ ―ç–Ω–Η―²–Β–Μ–Η–Β–Φ –Η –Φ–Β–Φ–±―Ä–Α–Ϋ–Ψ–Ι –ë―Ä―É―Ö–Α, –Α ―²–Α–Κ –Ε–Β –≤–Ϋ―É―²―Ä–Η –Φ–Β–Φ–±―Ä–Α–Ϋ―΄ –ë―Ä―É―Ö–Α. –û–Ϋ–Η ―¹–Ψ―¹―²–Ψ―è―² –Η–Ζ –Ψ―²–Μ–Ψ–Ε–Β–Ϋ–Η–Ι, –≤–Κ–Μ―é―΅–Α―é―â–Η―Ö –≤ ―¹–Β–±―è –Κ–Ψ–Ϋ–Β―΅–Ϋ―΄–Β –Ω―Ä–Ψ–¥―É–Κ―²―΄ –Φ–Β―²–Α–±–Ψ–Μ–Η–Ζ–Φ–Α, ―²–Α–Κ–Η–Β –Κ–Α–Κ –Α–Φ–Η–Μ–Ψ–Η–¥―΄, –Μ–Η–Ω–Ψ–Ω―Ä–Ψ―²–Β–Η–Ϋ―΄ –Η –¥―Ä―É–≥–Η–Β –≥–Η–¥―Ä–Ψ―³–Ψ–±–Ϋ―΄–Β –≤–Β―â–Β―¹―²–≤–Α. –Λ–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β –¥―Ä―É–Ζ –Φ–Ψ–Ε–Β―² –±―΄―²―¨ –Ω–Ψ―¹–Μ–Β–¥―¹―²–≤–Η–Β–Φ –Ϋ–Β–Ω–Ψ–Μ–Ϋ–Ψ–≥–Ψ ―Ä–Α–Ζ―Ä―É―à–Β–Ϋ–Η―è –Κ–Ψ–Ϋ–Β―΅–Ϋ―΄―Ö –Ω―Ä–Ψ–¥―É–Κ―²–Ψ–≤ –Φ–Β―²–Α–±–Ψ–Μ–Η–Ζ–Φ–Α, –Κ–Α–Κ ―³–Ψ―²–Ψ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤, ―²–Α–Κ –Η –Κ–Μ–Β―²–Ψ–Κ –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è. –Ξ–Ψ―²―è –±–Ψ–Μ–Β–Β –¥–Β―²–Α–Μ―¨–Ϋ―΄–Ι –Α–Ϋ–Α–Μ–Η–Ζ –±–Β–Μ–Κ–Ψ–≤–Ψ–≥–Ψ ―¹–Ψ―¹―²–Α–≤–Α –¥―Ä―É–Ζ –Ω―Ä–Η–≤–Β–Μ –Κ –Α–Μ―¨―²–Β―Ä–Ϋ–Α―²–Η–≤–Ϋ–Ψ–Ι ―²–Β–Ψ―Ä–Η–Η –Η―Ö ―³–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è. –Γ–Ψ–≥–Μ–Α―¹–Ϋ–Ψ ―ç―²–Ψ–Ι ―²–Β–Ψ―Ä–Η–Η, ―³–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β –¥―Ä―É–Ζ –Ϋ–Α―΅–Η–Ϋ–Α–Β―²―¹―è ―¹ –≥–Η–±–Β–Μ–Η –Κ–Μ–Β―²–Ψ–Κ –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è, –Κ–Ψ―²–Ψ―Ä–Α―è –Ω―Ä–Ψ–Η―¹―Ö–Ψ–¥–Η―² –≤―¹–Μ–Β–¥―¹―²–≤–Η–Β –≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –Ω―Ä–Ψ―Ü–Β―¹―¹–Α. –û–±―Ä–Α–Ζ―É―é―â–Α―è―¹―è –≤ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Β –±―Ä–Β―à―¨ –≤ ―ç–Ω–Η―²–Β–Μ–Η–Α–Μ―¨–Ϋ–Ψ–Φ –±–Α―Ä―¨–Β―Ä–Β –Α–Κ―²–Η–≤–Ϋ–Ψ –Ζ–Α―¹―²―Ä–Α–Η–≤–Α–Β―²―¹―è ―¹–Ψ―¹–Β–¥–Ϋ–Η–Φ–Η –Κ–Μ–Β―²–Κ–Α–Φ–Η –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è, –Κ–Ψ―²–Ψ―Ä―΄–Β ―¹–Β–Κ―Ä–Β―²–Η―Ä―É―é―² –Ϋ–Ψ–≤―΄–Ι –≤–Ϋ–Β–Κ–Μ–Β―²–Ψ―΅–Ϋ―΄–Ι –Φ–Α―²―Ä–Η–Κ―¹. –≠―²―É ―²–Β–Ψ―Ä–Η―é –Ω–Ψ–¥―²–≤–Β―Ä–Ε–¥–Α–Β―² –Ψ–±–Ϋ–Α―Ä―É–Ε–Β–Ϋ–Η–Β –Α–Κ―²–Η–≤–Ϋ―΄―Ö –¥–Β–Ϋ–¥―Ä–Η―²–Ϋ―΄―Ö –Κ–Μ–Β―²–Ψ–Κ –Η –Α–Κ―²–Η–≤–Ϋ―΄―Ö –Κ–Ψ–Φ–Ω–Ψ–Ϋ–Β–Ϋ―²–Ψ–≤ ―¹–Η―¹―²–Β–Φ―΄ –Κ–Ψ–Φ–Ω–Μ–Β–Φ–Β–Ϋ―²–Α –≤ –¥―Ä―É–Ζ–Α―Ö. –™–Η–¥―Ä–Ψ―³–Ψ–±–Ϋ―΄–Β –≤–Β―â–Β―¹―²–≤–Α –Η –Μ–Η–Ω–Ψ–Ω―Ä–Ψ―²–Β–Η–Ϋ―΄ –Φ–Ψ–≥―É―² –±―΄―²―¨ –Ψ―¹―²–Α―²–Κ–Α–Φ–Η –Ψ―Ä–≥–Α–Ϋ–Η―΅–Β―¹–Κ–Η―Ö –≤–Β―â–Β―¹―²–≤, –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–≤―à–Η―Ö―¹―è –Ω–Ψ―¹–Μ–Β –Ϋ–Β–Ω–Ψ–Μ–Ϋ–Ψ–≥–Ψ ―Ä–Α–Ζ―Ä―É―à–Β–Ϋ–Η―è –Κ–Μ–Β―²–Ψ–Κ.
II. –≠–Κ―¹―¹―É–¥–Α―²–Η–≤–Ϋ–Α―è (–Ϋ–Β–Ψ–≤–Α―¹–Κ―É–Μ―è―Ä–Ϋ–Α―è) ―³–Ψ―Ä–Φ–Α. –û–Ϋ–Α –Ω–Ψ–¥―Ä–Α–Ζ–¥–Β–Μ―è–Β―²―¹―è –Ϋ–Α 4 ―¹―²–Α–¥–Η–Η, –Ω–Ψ –Φ–Β―Ä–Β ―Ä–Α–Ζ–≤–Η―²–Η―è –Κ–Ψ―²–Ψ―Ä―΄―Ö –Ϋ–Α–±–Μ―é–¥–Α―é―²―¹―è ―Ä–Ψ―¹―² –Κ―Ä–Ψ–≤–Β–Ϋ–Ψ―¹–Ϋ―΄―Ö ―¹–Ψ―¹―É–¥–Ψ–≤ –≤ ―¹–Ψ―¹―É–¥–Η―¹―²–Ψ–Ι –Ψ–±–Ψ–Μ–Ψ―΅–Κ–Β –≥–Μ–Α–Ζ–Α, ―ç–Κ―¹―¹―É–¥–Α―²–Η–≤–Ϋ―΄–Ι –Ψ―²―ë–Κ –Η –Κ―Ä–Ψ–≤–Ψ–Η–Ζ–Μ–Η―è–Ϋ–Η―è –≤ ―¹–Β―²―΅–Α―²–Κ―É. –£ ―Ä–Α–Ζ–≤–Η―²–Η–Η –Ϋ–Β–Ψ–≤–Α―¹–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι ―³–Ψ―Ä–Φ―΄ –£–€–î –±–Ψ–Μ―¨―à–Ψ–Β –Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Β –Η–Φ–Β–Β―² ―³–Α–Κ―²–Ψ―Ä ―Ä–Ψ―¹―²–Α ―ç–Ϋ–¥–Ψ―²–Β–Μ–Η―è ―¹–Ψ―¹―É–¥–Ψ–≤ (vascular endothelial growth factor - VEGF), –Κ–Ψ―²–Ψ―Ä―΄–Ι ―¹–Β–Κ―Ä–Β―²–Η―Ä―É–Β―²―¹―è –Κ–Μ–Β―²–Κ–Α–Φ–Η ―Ä–Β―²–Η–Ϋ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è. VEGF βÄ™ –Ψ―¹–Ϋ–Ψ–≤–Ϋ–Ψ–Ι –Α–Ϋ–≥–Η–Ψ–≥–Β–Ϋ–Ϋ―΄–Ι ―³–Α–Κ―²–Ψ―Ä, –≤ –Ϋ–Ψ―Ä–Φ–Β ―¹–Η–Ϋ―²–Β–Ζ–Η―Ä―É–Β–Φ―΄–Ι –≤ –Φ–Α–Μ―΄―Ö –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Α―Ö. –ü―Ä–Η –≥–Η–Ω–Ψ–Κ―¹–Η–Η ―¹–Η–Ϋ―²–Β–Ζ ―³–Α–Κ―²–Ψ―Ä–Α VEGF –≤ –Κ–Μ–Β―²–Κ–Α―Ö –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ ―É–≤–Β–Μ–Η―΅–Η–≤–Α–Β―²―¹―è. –û–Ϋ ―¹–Β–Κ―Ä–Β―²–Η―Ä―É–Β―²―¹―è ―¹ –±–Α–Ζ–Α–Μ―¨–Ϋ–Ψ–Ι ―΅–Α―¹―²–Η –Κ–Μ–Β―²–Ψ–Κ –≤ –Φ–Β–Ε–Κ–Μ–Β―²–Ψ―΅–Ϋ―΄–Ι –Φ–Α―²―Ä–Η–Κ―¹, –Α –Ζ–Α―²–Β–Φ –Ω―Ä–Ψ–Ϋ–Η–Κ–Α–Β―² ―΅–Β―Ä–Β–Ζ –Φ–Β–Φ–±―Ä–Α–Ϋ―É –ë―Ä―É―Ö–Α –Κ ―¹–Ψ―¹―É–¥–Α–Φ ―Ö–Ψ―Ä–Η–Ψ–Η–¥–Β–Η. –Γ–≤―è–Ζ―΄–≤–Α―è―¹―¨ ―¹ –Κ–Μ–Β―²–Κ–Α–Φ–Η ―ç–Ϋ–¥–Ψ―²–Β–Μ–Η―è ―Ö–Ψ―Ä–Η–Ψ–Κ–Α–Ω–Η–Μ–Μ―è―Ä–Ψ–≤, VEGF –Ζ–Α–Ω―É―¹–Κ–Α–Β―² ―¹–Η–≥–Ϋ–Α–Μ―¨–Ϋ―΄–Ι –Κ–Α―¹–Κ–Α–¥, –Κ–Ψ―²–Ψ―Ä―΄–Ι –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ ―¹–Η–Ϋ―²–Β–Ζ―É –±–Β–Μ–Κ–Ψ–≤, –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä―É―é―â–Η―Ö –Κ–Μ–Β―²–Ψ―΅–Ϋ―É―é –Ω―Ä–Ψ–Μ–Η―³–Β―Ä–Α―Ü–Η―é. –≠―²–Ψ –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ –Ω―Ä–Ψ―Ä–Α―¹―²–Α–Ϋ–Η―é –Α–Ϋ–Ψ–Φ–Α–Μ―¨–Ϋ―΄―Ö ―¹–Ψ―¹―É–¥–Ψ–≤ –≤–≥–Μ―É–±―¨ ―¹–Β―²―΅–Α―²–Κ–Η. –ü–Α―²–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Ι –Α–Ϋ–≥–Η–Ψ–≥–Β–Ϋ–Β–Ζ, –≤ –Κ–Ψ–Ϋ–Β―΅–Ϋ–Ψ–Φ –Η―²–Ψ–≥–Β, –≤–Β–¥–Β―² –Κ ―³–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Ϋ–Η―é –Ψ―²–Β–Κ–Α, –Κ―Ä–Ψ–≤–Ψ–Η–Ζ–Μ–Η―è–Ϋ–Η―é –≤ ―¹–Β―²―΅–Α―²–Κ―É, –Β–Β –Ψ―²―¹–Μ–Ψ–Ι–Κ–Β. –Δ–Α–Κ–Η–Β –Ψ―¹–Μ–Ψ–Ε–Ϋ–Β–Ϋ–Η―è –Ϋ–Β–Ψ–≤–Α―¹–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –£–€–î ―è–≤–Μ―è―é―²―¹―è –Ϋ–Α–Η–±–Ψ–Μ–Β–Β –Ψ–Ω–Α―¹–Ϋ―΄–Φ–Η –Η –Φ–Ψ–≥―É―² –Ω―Ä–Η–≤–Β―¹―²–Η –Κ –Ω–Ψ―²–Β―Ä–Β –Ζ―Ä–Β–Ϋ–Η―è.
III. –†―É–±―Ü–Ψ–≤–Α―è ―³–Ψ―Ä–Φ–Α, –Ζ–Α–Κ–Α–Ϋ―΅–Η–≤–Α―é―â–Α―è―¹―è ―³–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β–Φ –¥–Η―¹–Κ–Ψ–≤–Η–¥–Ϋ–Ψ–≥–Ψ ―³–Η–±―Ä–Ψ–Ζ–Ϋ–Ψ–≥–Ψ ―Ä―É–±―Ü–Α.
–û–±―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, ―¹―²―Ä–Α–¥–Α―é―â–Η―Ö –≤–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Ψ–Ι –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η–Β–Ι, –≤–Κ–Μ―é―΅–Α–Β―² –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Η–Β –Ψ―¹―²―Ä–Ψ―²―΄ –Ζ―Ä–Β–Ϋ–Η―è –Η –±–Η–Ψ–Φ–Η–Κ―Ä–Ψ―¹–Κ–Ψ–Ω–Η―é, –Κ–Ψ―²–Ψ―Ä―É―é –Ω―Ä–Ψ–≤–Ψ–¥―è―² –¥–Μ―è –≤―΄―è–≤–Μ–Β–Ϋ–Η―è –¥―Ä―É–≥–Η―Ö –Ω―Ä–Η―΅–Η–Ϋ –Ω–Ψ―è–≤–Μ–Β–Ϋ–Η―è ―¹–Η–Φ–Ω―²–Ψ–Φ–Α―²–Η–Κ–Η (–Ϋ–Α–Ω―Ä–Η–Φ–Β―Ä, –¥–Μ―è –¥–Η―³―³–Β―Ä–Β–Ϋ―Ü–Η―Ä–Ψ–≤–Κ–Η ―¹ –≤–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Ψ–Ι –Κ–Α―²–Α―Ä–Α–Κ―²–Ψ–Ι). –î–Μ―è –¥–Η–Α–≥–Ϋ–Ψ―¹―²–Η–Κ–Η –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è –Ω―Ä–Η–Φ–Β–Ϋ―è―é―²―¹―è –¥–≤–Α –Ψ―¹–Ϋ–Ψ–≤–Ϋ―΄―Ö –Φ–Β―²–Ψ–¥–Α βÄ™ ―³–Μ―é–Ψ―Ä–Β―¹―Ü–Β–Ϋ―²–Ϋ–Α―è –Α–Ϋ–≥–Η–Ψ–≥―Ä–Α―³–Η―è –Η –Ψ―¹–Φ–Ψ―²―Ä –≥–Μ–Α–Ζ–Ϋ–Ψ–≥–Ψ –¥–Ϋ–Α, –Ω–Ψ–Ζ–≤–Ψ–Μ―è―é―â–Α―è –Ϋ–Β ―²–Ψ–Μ―¨–Κ–Ψ –¥–Η―³―³–Β―Ä–Β–Ϋ―Ü–Η―Ä–Ψ–≤–Α―²―¨ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η–Β, –Ϋ–Ψ –Η –≤―΄―è–≤–Η―²―¨ ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Β ―³–Ψ―Ä–Φ―΄ –£–€–î [10]. –ß–Α―¹―²–Ψ –Ω–Α―Ü–Η–Β–Ϋ―²–Α–Φ –Ω―Ä–Β–¥–Μ–Α–≥–Α–Β―²―¹―è –Ω―Ä–Ψ–Ι―²–Η –Φ–Η–Ϋ―É―²–Ϋ―΄–Ι ―²–Β―¹―² βÄ™ ―¹–Β―²–Κ―É –ê–Φ―¹–Μ–Β―Ä–Α. –‰―¹–Κ–Α–Ε–Β–Ϋ–Η–Β –≤–Β―Ä―²–Η–Κ–Α–Μ―¨–Ϋ―΄―Ö –Η–Μ–Η –≥–Ψ―Ä–Η–Ζ–Ψ–Ϋ―²–Α–Μ―¨–Ϋ―΄―Ö –Μ–Η–Ϋ–Η–Ι βÄ™ –Φ–Β―²–Α–Φ–Ψ―Ä―³–Ψ–Ω―¹–Η–Η, –Α ―²–Α–Κ–Ε–Β ―Ä–Α―¹–Ω–Μ―΄–≤―΅–Η–≤–Ψ―¹―²―¨ –Κ–Ψ–Ϋ―²―É―Ä–Ψ–≤ ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ–Ψ–Ι ―²–Ψ―΅–Κ–Η –Φ–Ψ–≥―É―² ―¹–≤–Η–¥–Β―²–Β–Μ―¨―¹―²–≤–Ψ–≤–Α―²―¨ –Ψ ―Ä–Α–Ζ–≤–Η―²–Η–Η –≤–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Ψ–Ι –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η–Η.
–ù–Α ―¹―²–Α–¥–Η–Η –Ω–Ψ―è–≤–Μ–Β–Ϋ–Η―è –Φ―è–≥–Κ–Η―Ö –¥―Ä―É–Ζ, –Κ–Ψ―²–Ψ―Ä―΄–Β –≤―΄―è–≤–Μ―è―é―²―¹―è –Ψ―³―²–Α–Μ―¨–Φ–Ψ―¹–Κ–Ψ–Ω–Η―΅–Β―¹–Κ–Η –Η ―è–≤–Μ―è―é―²―¹―è ―¹–Α–Φ―΄–Φ –Ω–Β―Ä–≤―΄–Φ ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–Φ –£–€–î, –Ω–Α―Ü–Η–Β–Ϋ―²―É ―Ä–Β–Κ–Ψ–Φ–Β–Ϋ–¥―É–Β―²―¹―è –Ω―Ä–Ψ–≤–Ψ–¥–Η―²―¨ –Β–Ε–Β–¥–Ϋ–Β–≤–Ϋ―΄–Ι ―¹–Α–Φ–Ψ–Κ–Ψ–Ϋ―²―Ä–Ψ–Μ―¨ –Ω―Ä–Η –Ω–Ψ–Φ–Ψ―â–Η ―¹–Β―²–Κ–Η –ê–Φ―¹–Μ–Β―Ä–Α –Η –Ψ–±―è–Ζ–Α―²–Β–Μ―¨–Ϋ–Ψ–Β –Ω–Ψ―¹–Β―â–Β–Ϋ–Η–Β –Ψ―³―²–Α–Μ―¨–Φ–Ψ–Μ–Ψ–≥–Α –≤ ―¹–Μ―É―΅–Α–Β –Ω–Ψ―è–≤–Μ–Β–Ϋ–Η―è –Ϋ–Ψ–≤―΄―Ö ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–≤ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è.
–ù–Β―¹–Φ–Ψ―²―Ä―è –Ϋ–Α ―Ä–Α–Ζ―Ä–Α–±–Ψ―²–Κ―É –Φ–Ϋ–Ψ–Ε–Β―¹―²–≤–Α –Ω–Ψ–¥―Ö–Ψ–¥–Ψ–≤ –Κ –Μ–Β―΅–Β–Ϋ–Η―é –Η –Α–Κ―²–Η–≤–Ϋ―΄–Ι –Ω–Ψ–Η―¹–Κ –Φ–Η―à–Β–Ϋ–Β–Ι –Μ–Β–Κ–Α―Ä―¹―²–≤–Β–Ϋ–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Η, ―ç―³―³–Β–Κ―²–Η–≤–Ϋ―΄―Ö –Φ–Β―²–Ψ–¥–Ψ–≤ –Μ–Β―΅–Β–Ϋ–Η―è –£–€–î –Ϋ–Β –Ϋ–Α–Ι–¥–Β–Ϋ–Ψ. –£―¹–Β ―¹―É―â–Β―¹―²–≤―É―é―â–Η–Β –Φ–Β―²–Ψ–¥―΄ –Μ–Β―΅–Β–Ϋ–Η―è –Ϋ–Ψ―¹―è―² –Μ–Η―à―¨ –Ω–Ψ–¥–¥–Β―Ä–Ε–Η–≤–Α―é―â–Η–Ι ―Ö–Α―Ä–Α–Κ―²–Β―Ä, ―²–Ψ –Β―¹―²―¨, –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ―΄ –Ϋ–Α –Ω―Ä–Β–¥–Ψ―²–≤―Ä–Α―â–Β–Ϋ–Η–Β –¥–Α–Μ―¨–Ϋ–Β–Ι―à–Β–Ι –Ω–Ψ―²–Β―Ä–Η –Ζ―Ä–Β–Ϋ–Η―è, –Α –Ϋ–Β –Ϋ–Α –Β–≥–Ψ ―É–Μ―É―΅―à–Β–Ϋ–Η–Β. –Π–Β–Μ–Η –Μ–Β―΅–Β–Ϋ–Η―è ―¹–≤–Ψ–¥―è―²―¹―è, –Ω―Ä–Β–Ε–¥–Β –≤―¹–Β–≥–Ψ, –Κ –Ω―Ä–Β–¥―É–Ω―Ä–Β–Ε–¥–Β–Ϋ–Η―é –Ψ―¹–Μ–Ψ–Ε–Ϋ–Β–Ϋ–Η–Ι (–Ω―Ä–Η –Α―²―Ä–Ψ―³–Η―΅–Β―¹–Κ–Ψ–Ι ―³–Ψ―Ä–Φ–Β βÄ™ –Ω–Ψ―è–≤–Μ–Β–Ϋ–Η―é ―¹―É–±―Ä–Β―²–Η–Ϋ–Α–Μ―¨–Ϋ–Ψ–Ι –Ϋ–Β–Ψ–≤–Α―¹–Κ―É–Μ―è―Ä–Η–Ζ–Α―Ü–Η–Η, –Ω―Ä–Η ―ç–Κ―¹―¹―É–¥–Α―²–Η–≤–Ϋ–Ψ–Ι βÄ™ –≤–Ψ–Ζ–Ϋ–Η–Κ–Ϋ–Ψ–≤–Β–Ϋ–Η―é –Κ―Ä–Ψ–≤–Ψ–Η–Ζ–Μ–Η―è–Ϋ–Η–Ι –≤ ―¹–Β―²―΅–Α―²–Κ―É ―Ä–Α–Ζ–Μ–Η―΅–Ϋ–Ψ–Ι –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η–Η).
–ù–Α ―¹–Β–≥–Ψ–¥–Ϋ―è―à–Ϋ–Η–Ι –¥–Β–Ϋ―¨ –Κ –Ψ―¹–Ϋ–Ψ–≤–Ϋ―΄–Φ ―¹–Ω–Ψ―¹–Ψ–±–Α–Φ –Μ–Β―΅–Β–Ϋ–Η―è –£–€–î –Ψ―²–Ϋ–Ψ―¹―è―² –Η–Ϋ―²―Ä–Α–≤–Η―²―Ä–Β–Α–Μ―¨–Ϋ―É―é –Α–Ϋ―²–Η-VEGF ―²–Β―Ä–Α–Ω–Η―é, ―³–Ψ―²–Ψ–¥–Η–Ϋ–Α–Φ–Η―΅–Β―¹–Κ―É―é ―²–Β―Ä–Α–Ω–Η―é ―¹―É–±―³–Ψ–≤–Β–Α–Μ―¨–Ϋ―΄―Ö –Ψ―΅–Α–≥–Ψ–≤ –Η ―³–Ψ―²–Ψ–Κ–Ψ–Α–≥―É–Μ―è―Ü–Η―é –Α―Ä–≥–Ψ–Ϋ–Ψ–≤―΄–Φ –Μ–Α–Ζ–Β―Ä–Ψ–Φ ―Ö–Ψ―Ä–Η–Ψ–Η–¥–Α–Μ―¨–Ϋ–Ψ–Ι –Ϋ–Β–Ψ–≤–Α―¹–Κ―É–Μ―è―Ä–Η–Ζ–Α―Ü–Η–Η [11]. –ü―Ä–Η―΅―ë–Φ –¥–Ψ –Ϋ–Β–¥–Α–≤–Ϋ–Η―Ö –Ω–Ψ―Ä ―²–Β―Ä–Φ–Η―΅–Β―¹–Κ–Α―è –Μ–Α–Ζ–Β―Ä–Ϋ–Α―è ―³–Ψ―²–Ψ–Κ–Ψ–Α–≥―É–Μ―è―Ü–Η―è ―¹―΅–Η―²–Α–Μ–Α―¹―¨ –Β–¥–Η–Ϋ―¹―²–≤–Β–Ϋ–Ϋ–Ψ–Ι –Ψ–±―â–Β–Ω―Ä–Η–Ϋ―è―²–Ψ–Ι ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ–Ι –Φ–Β―²–Ψ–¥–Η–Κ–Ψ–Ι, ―à–Η―Ä–Ψ–Κ–Ψ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–≤―à–Β–Ι―¹―è –¥–Μ―è –Μ–Β―΅–Β–Ϋ–Η―è –£–€–î. –ü―Ä–Η –¥–Α–Ϋ–Ϋ–Ψ–Φ –≤–Η–¥–Β –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α –Μ―É―΅ –Α―Ä–≥–Ψ–Ϋ–Ψ–≤–Ψ–≥–Ψ –Η–Μ–Η –¥―Ä―É–≥–Ψ–≥–Ψ –Μ–Α–Ζ–Β―Ä–Α –≤–Η–¥–Η–Φ–Ψ–≥–Ψ ―¹–Ω–Β–Κ―²―Ä–Α ―¹ –Ω–Ψ–Φ–Ψ―â―¨―é ―â–Β–Μ–Β–≤–Ψ–Ι –Μ–Α–Φ–Ω―΄ –Ϋ–Α–Ω―Ä–Α–≤–Μ―è―é―² –Κ –Ψ–±–Μ–Α―¹―²–Η ―Ö–Ψ―Ä–Η–Ψ–Η–¥–Α–Μ―¨–Ϋ–Ψ–Ι –Ϋ–Β–Ψ–≤–Α―¹–Κ―É–Μ―è―Ä–Η–Ζ–Α―Ü–Η–Η, –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Ϋ–Ψ–Ι ―¹ –Ω–Ψ–Φ–Ψ―â―¨―é –Α–Ϋ–≥–Η–Ψ–≥―Ä–Α―³–Η–Η. –≠–Ϋ–Β―Ä–≥–Η―è –Μ–Α–Ζ–Β―Ä–Α –Α–±―¹–Ψ―Ä–±–Η―Ä―É–Β―²―¹―è, –≥–Μ–Α–≤–Ϋ―΄–Φ –Ψ–±―Ä–Α–Ζ–Ψ–Φ, –Φ–Β–Μ–Α–Ϋ–Η–Ϋ–Ψ–≤―΄–Φ –Ω–Η–≥–Φ–Β–Ϋ―²–Ψ–Φ ―Ä–Β―²–Η–Ϋ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è, –Α –Ψ―¹―²–Α–≤―à–Α―è―¹―è ―²–Β–Ω–Μ–Ψ–≤–Α―è ―ç–Ϋ–Β―Ä–≥–Η―è –Κ–Ψ–Α–≥―É–Μ–Η―Ä―É–Β―² –Η ―Ä–Α–Ζ―Ä―É―à–Α–Β―² ―Ä―è–¥–Ψ–Φ –Μ–Β–Ε–Α―â–Η–Β ―¹–Ψ―¹―É–¥―΄ –Ϋ–Β–Ψ–≤–Α―¹–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –Φ–Β–Φ–±―Ä–Α–Ϋ―΄. –Π–Β–Μ―¨―é –¥–Α–Ϋ–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Η ―è–≤–Μ―è–Β―²―¹―è –Ψ–≥―Ä–Α–Ϋ–Η―΅–Β–Ϋ–Η–Β ―¹–Κ–Ψ―²–Ψ–Φ―΄, ―²–Α–Κ ―΅―²–Ψ–±―΄ –Κ–Ψ–Ϋ–Β―΅–Ϋ―΄–Ι –Β–Β ―Ä–Α–Ζ–Φ–Β―Ä ―¹―²–Α–Μ –Φ–Β–Ϋ―¨―à–Β, ―΅–Β–Φ ―Ä–Α–Ζ–Φ–Β―Ä ―¹–Κ–Ψ―²–Ψ–Φ―΄ –±–Β–Ζ –Μ–Β―΅–Β–Ϋ–Η―è [12]. –ê–Μ―¨―²–Β―Ä–Ϋ–Α―²–Η–≤–Ψ–Ι –Μ–Α–Ζ–Β―Ä–Ψ–Κ–Ψ–Α–≥―É–Μ―è―Ü–Η–Η ―¹―²–Α–Μ–Α ―³–Ψ―²–Ψ–¥–Η–Ϋ–Α–Φ–Η―΅–Β―¹–Κ–Α―è ―²–Β―Ä–Α–Ω–Η―è (–Λ–Δ–î). –Λ–î–Δ –Ψ–±―É―¹–Μ–Ψ–≤–Μ–Β–Ϋ–Α ―¹–Ω–Ψ―¹–Ψ–±–Ϋ–Ψ―¹―²―¨―é ―³–Ψ―²–Ψ―¹–Β–Ϋ―¹–Η–±–Η–Μ–Η–Ζ–Α―²–Ψ―Ä–Α –Η–Ζ–±–Η―Ä–Α―²–Β–Μ―¨–Ϋ–Ψ –Ϋ–Α–Κ–Α–Ω–Μ–Η–≤–Α―²―¨―¹―è –≤ –¥–Β–Μ―è―â–Η―Ö―¹―è –Κ–Μ–Β―²–Κ–Α―Ö –Η –Ω―Ä–Η –≤–Ψ–Ζ–¥–Β–Ι―¹―²–≤–Η–Η ―¹–≤–Β―²–Α ―¹ –¥–Μ–Η–Ϋ–Ψ–Ι –≤–Ψ–Μ–Ϋ―΄, ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤―É―é―â–Β–Ι –Ω–Η–Κ―É –Ω–Ψ–≥–Μ–Ψ―â–Β–Ϋ–Η―è ―³–Ψ―²–Ψ―¹–Β–Ϋ―¹–Η–±–Η–Μ–Η–Ζ–Α―²–Ψ―Ä–Α, –≥–Β–Ϋ–Β―Ä–Η―Ä–Ψ–≤–Α―²―¨ ―¹–Η–Ϋ–≥–Μ–Β―²–Ϋ―΄–Ι –Κ–Η―¹–Μ–Ψ―Ä–Ψ–¥ –Η –¥―Ä―É–≥–Η–Β –Α–Κ―²–Η–≤–Ϋ―΄–Β ―Ä–Α–¥–Η–Κ–Α–Μ―΄, –Ψ–Κ–Α–Ζ―΄–≤–Α―é―â–Η–Β ―Ü–Η―²–Ψ―²–Ψ–Κ―¹–Η―΅–Β―¹–Κ–Η–Ι ―ç―³―³–Β–Κ―². –ö―Ä–Ψ–Φ–Β ―²–Ψ–≥–Ψ, –Λ–î–Δ –≤―΄–Ζ―΄–≤–Α–Β―² ―³–Ψ―²–Ψ–¥–Η–Ϋ–Α–Φ–Η―΅–Β―¹–Κ―É―é –Ψ–Κ–Κ–Μ―é–Ζ–Η―é –Ϋ–Ψ–≤–Ψ–Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Ϋ―΄―Ö ―¹–Ψ―¹―É–¥–Ψ–≤ ―¹ ―¹–Ψ―Ö―Ä–Α–Ϋ–Β–Ϋ–Η–Β–Φ –Ψ–Κ―Ä―É–Ε–Α―é―â–Η―Ö ―¹―²―Ä―É–Κ―²―É―Ä (―¹–Β―²―΅–Α―²–Κ–Η, –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è, ―Ö–Ψ―Ä–Η–Ψ–Κ–Α–Ω–Η–Μ–Μ―è―Ä–Ψ–≤). –ü―Ä–Η –Μ–Β―΅–Β–Ϋ–Η–Η –Η―¹–Ω–Ψ–Μ―¨–Ζ―É―é―² ―³–Ψ―²–Ψ―¹–Β–Ϋ―¹–Η–±–Η–Μ–Η–Ζ–Α―²–Ψ―Ä –¥–Μ―è –≤–Ϋ―É―²―Ä–Η–≤–Β–Ϋ–Ϋ–Ψ–≥–Ψ –≤–≤–Β–¥–Β–Ϋ–Η―è –≤–Β―Ä―²–Β–Ω–Ψ―Ä―³–Η―Ä–Η–Ϋ (–≤–Η–Ζ―É–¥–Η–Ϋ), ―Ä–Α–Ζ―Ä–Β―à―ë–Ϋ–Ϋ―΄–Ι –Κ –Ω―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η―é –≤ –†–Ψ―¹―¹–Η–Η. –ù–Α–Η–±–Ψ–Μ–Β–Β –Ω–Β―Ä―¹–Ω–Β–Κ―²–Η–≤–Ϋ―΄–Φ –Η–Ζ ―²―Ä–Β―Ö –Ω–Β―Ä–Β―΅–Η―¹–Μ–Β–Ϋ–Ϋ―΄―Ö –Φ–Β―²–Ψ–¥–Ψ–≤ –Μ–Β―΅–Β–Ϋ–Η―è ―è–≤–Μ―è–Β―²―¹―è –Η–Ϋ―²―Ä–Α–≤–Η―²―Ä–Β–Α–Μ―¨–Ϋ–Ψ–Β –≤–≤–Β–¥–Β–Ϋ–Η–Β –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤, –Η–Ϋ–≥–Η–±–Η―Ä―É―é―â–Η―Ö –Α–Ϋ–≥–Η–Ψ–≥–Β–Ϋ–Β–Ζ, –Α –Η–Φ–Β–Ϋ–Ϋ–Ψ ―¹–≤―è–Ζ―΄–≤–Α―é―â–Η―Ö ―³–Α–Κ―²–Ψ―Ä ―Ä–Ψ―¹―²–Α ―ç–Ϋ–¥–Ψ―²–Β–Μ–Η―è ―¹–Ψ―¹―É–¥–Ψ–≤. –£ –Κ–Μ–Η–Ϋ–Η–Κ–Β –Ϋ–Α ―¹–Β–≥–Ψ–¥–Ϋ―è―à–Ϋ–Η–Ι –¥–Β–Ϋ―¨ –Η―¹–Ω–Ψ–Μ―¨–Ζ―É―é―²―¹―è –Ϋ–Β―¹–Κ–Ψ–Μ―¨–Κ–Ψ ―²–Α–Κ–Η―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤: –Ω–Β–≥–Α–Ω―²–Α–Ϋ–Η–± (–Ψ–Μ–Η–≥–Ψ–Ϋ―É–Κ–Μ–Β–Ψ―²–Η–¥), ―¹–≤―è–Ζ―΄–≤–Α―é―â–Η–Ι –Ψ–¥–Ϋ―É –Η–Ζ–Ψ―³–Ψ―Ä–Φ―É VEGF165, ―Ä–Α–Ϋ–Η–±–Η–Ζ―É–Φ–Α–± (―³―Ä–Α–≥–Φ–Β–Ϋ―² –Φ–Ψ–Ϋ–Ψ–Κ–Μ–Ψ–Ϋ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Α–Ϋ―²–Η―²–Β–Μ–Α –Κ VEGF) –Η –±–Β–≤–Α―Ü–Η–Ζ―É–Φ–Α–± (–Ω–Ψ–Μ–Ϋ–Ψ–Β –Α–Ϋ―²–Η―²–Β–Μ–Ψ –Κ VEGF), –Ω―Ä–Η–Φ–Β–Ϋ―è–Β–Φ―΄–Ι –≤ ―Ä–Α–Φ–Κ–Α―Ö –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Η―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Ι [13].
–Δ–Α–Κ–Η–Β ―¹–Ω–Ψ―¹–Ψ–±―΄ –Μ–Β―΅–Β–Ϋ–Η―è –Κ–Α–Κ ―Ä–Α–¥–Η–Ψ―²–Β―Ä–Α–Ω–Η―è –Η ―²―Ä–Α–Ϋ―¹–Ω―É–Ω–Ω–Η–Μ―è―Ä–Ϋ–Α―è ―²–Β―Ä–Φ–Ψ―²–Β―Ä–Α–Ω–Η―è –Ϋ–Α ―¹–Β–≥–Ψ–¥–Ϋ―è―à–Ϋ–Η–Ι –¥–Β–Ϋ―¨ ―¹―É―â–Β―¹―²–≤–Β–Ϋ–Ϋ–Ψ–Ι ―Ä–Ψ–Μ–Η –≤ –Μ–Β―΅–Β–Ϋ–Η–Η –£–€–î –Ϋ–Β –Η–≥―Ä–Α―é―². –Ξ–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Η–Β –Φ–Β―²–Ψ–¥–Η–Κ–Η, –≤–Κ–Μ―é―΅–Α―é―â–Η–Β ―É–¥–Α–Μ–Β–Ϋ–Η–Β ―¹―É–±―Ä–Β―²–Η–Ϋ–Α–Μ―¨–Ϋ―΄―Ö –Ϋ–Β–Ψ–≤–Α―¹–Κ―É–Μ―è―Ä–Ϋ―΄―Ö –Φ–Β–Φ–±―Ä–Α–Ϋ, –≤ –Ϋ–Α―¹―²–Ψ―è―â–Β–Β –≤―Ä–Β–Φ―è –Ϋ–Α―Ö–Ψ–¥―è―²―¹―è –Ϋ–Α ―¹―²–Α–¥–Η–Η ―ç–Κ―¹–Ω–Β―Ä–Η–Φ–Β–Ϋ―²–Α –Η ―è–≤–Μ―è―é―²―¹―è –¥–Ψ―¹―²―É–Ω–Ϋ―΄–Φ–Η –Μ–Η―à―¨ –≤ –Ϋ–Β–Κ–Ψ―²–Ψ―Ä―΄―Ö –Κ–Μ–Η–Ϋ–Η–Κ–Α―Ö.
–‰–Ζ–≤–Β―¹―²–Ϋ–Ψ, ―΅―²–Ψ –≤ ―Ä–Α–Ζ–≤–Η―²–Η–Η –£–€–î –±–Ψ–Μ―¨―à–Ψ–Β –Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Β –Η–Φ–Β―é―² –Ψ–Κ–Η―¹–Μ–Η―²–Β–Μ―¨–Ϋ―΄–Ι ―¹―²―Ä–Β―¹―¹ –Η –Ω–Ψ–≤―Ä–Β–Ε–¥–Α―é―â–Β–Β –¥–Β–Ι―¹―²–≤–Η–Β ―¹–Η–Ϋ–Β–≥–Ψ ―¹–≤–Β―²–Α. –£ ―¹–≤―è–Ζ–Η ―¹ ―ç―²–Η–Φ –≤ –Ω–Ψ―¹–Μ–Β–¥–Ϋ–Β–Β –≤―Ä–Β–Φ―è ―à–Η―Ä–Ψ–Κ–Ψ–Β –Ω―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η–Β –Ω–Ψ–Μ―É―΅–Η–Μ–Ψ ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η–Β –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤, ―¹–Ψ–¥–Β―Ä–Ε–Α―â–Η―Ö –Κ–Α―Ä–Ψ―²–Η–Ϋ–Ψ–Η–¥―΄ - –Μ―é―²–Β–Η–Ϋ –Η –Ζ–Β–Α–Κ―¹–Α–Ϋ―²–Η–Ϋ. –û–Ϋ–Η –Ϋ–Α–Κ–Α–Ω–Μ–Η–≤–Α―é―²―¹―è –≤ –Φ–Α–Κ―É–Μ–Β –Η –Ψ–±―Ä–Α–Ζ―É―é―² –Φ–Α–Κ―É–Μ―è―Ä–Ϋ―΄–Ι –Ω–Η–≥–Φ–Β–Ϋ―². –€–Α–Κ―É–Μ―è―Ä–Ϋ―΄–Ι ―Ä–Α–¥–Η–Κ–Α–Μ―΄. –û–Ϋ –Ε–Β–Μ―²–Ψ–≥–Ψ ―Ü–≤–Β―²–Α –Η –Ω–Ψ―ç―²–Ψ–Φ―É –Α–±―¹–Ψ―Ä–±–Η―Ä―É–Β―² ―¹–Η–Ϋ–Η–Ι ―¹–≤–Β―². –ü–Ψ―¹–Κ–Ψ–Μ―¨–Κ―É –Η–Ζ–≤–Β―¹―²–Ϋ–Ψ, ―΅―²–Ψ ―¹–Η–Ϋ–Η–Ι ―¹–≤–Β―² –Η ―¹–≤–Ψ–±–Ψ–¥–Ϋ―΄–Β ―Ä–Α–¥–Η–Κ–Α–Μ―΄ ―¹–Ω–Ψ―¹–Ψ–±―¹―²–≤―É―é―² ―Ä–Α–Ζ–≤–Η―²–Η―é –£–€–î, –≤–Ω–Ψ–Μ–Ϋ–Β –Ψ―΅–Β–≤–Η–¥–Ϋ–Ψ, ―΅―²–Ψ ―ç―²–Ψ―² –Ω–Η–≥–Φ–Β–Ϋ―² –Φ–Ψ–Ε–Β―² ―¹―΄–≥―Ä–Α―²―¨ –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Ϋ―É―é ―Ä–Ψ–Μ―¨ –≤ –Ζ–Α―â–Η―²–Β –Ψ―² ―ç―²–Ψ–Ι –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Η [14]. –£ –Ϋ–Α―¹―²–Ψ―è―â–Β–Β –≤―Ä–Β–Φ―è –≤ –Γ–®–ê –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–Φ –Ϋ–Ψ–Φ–Β―Ä –Ψ–¥–Η–Ϋ, –Ω―Ä–Η–Φ–Β–Ϋ―è–Β–Φ―΄–Φ –¥–Μ―è –Ω―Ä–Ψ―³–Η–Μ–Α–Κ―²–Η–Κ–Η –Η –Μ–Β―΅–Β–Ϋ–Η―è –£–€–î, ―è–≤–Μ―è–Β―²―¹―è ¬Ϊ–û–Κ―É–≤–Α–Ι―² –¦―é―²–Β–Η–Ϋ¬Μ. –Λ–Ψ―Ä–Φ―É–Μ–Α –û–Κ―É–≤–Α–Ι―² –¦―é―²–Β–Η–Ϋ–Α –≤–Κ–Μ―é―΅–Α–Β―² –≤ ―¹–Β–±―è –Κ–Α–Κ –≤–Ψ–¥–Ψ-, ―²–Α–Κ –Η –Ε–Η―Ä–Ψ―Ä–Α―¹―²–≤–Ψ―Ä–Η–Φ―΄–Β –Κ–Ψ–Φ–Ω–Ψ–Ϋ–Β–Ϋ―²―΄: –Κ–Α―Ä–Ψ―²–Η–Ϋ–Ψ–Η–¥―΄ (–Μ―é―²–Β–Η–Ϋ –Η –Ζ–Β–Α–Κ―¹–Α–Ϋ―²–Η–Ϋ), –≤–Η―²–Α–Φ–Η–Ϋ―΄-–Α–Ϋ―²–Η–Ψ–Κ―¹–Η–¥–Α–Ϋ―²―΄ (–Γ –Η –ï), –Φ–Η–Κ―Ä–Ψ―ç–Μ–Β–Φ–Β–Ϋ―²―΄ (―Ü–Η–Ϋ–Κ –Η ―¹–Β–Μ–Β–Ϋ). –ü―Ä–Α–Κ―²–Η–Κ–Α –Ω–Ψ–Κ–Α–Ζ―΄–≤–Α–Β―², ―΅―²–Ψ –Ϋ–Α–Η–Μ―É―΅―à–Β–Β –≤―¹–Α―¹―΄–≤–Α–Ϋ–Η–Β –Η–Ϋ–≥―Ä–Β–¥–Η–Β–Ϋ―²–Ψ–≤ –Ω―Ä–Ψ–Η―¹―Ö–Ψ–¥–Η―² –≤ –Ϋ–Β–±–Ψ–Μ―¨―à–Η―Ö –¥–Ψ–Ζ–Α―Ö, ―É―΅―²–Β–Ϋ–Ϋ―΄―Ö –Ω―Ä–Η –Ω―Ä–Ψ–Η–Ζ–≤–Ψ–¥―¹―²–≤–Β –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α. –û–Κ―É–≤–Α–Ι―² –¦―é―²–Β–Η–Ϋ –Ω―Ä–Β–Κ―Ä–Α―¹–Ϋ–Ψ –Ζ–Α―Ä–Β–Κ–Ψ–Φ–Β–Ϋ–¥–Ψ–≤–Α–Μ ―¹–Β–±―è –≤ –Φ–Ϋ–Ψ–≥–Ψ―΅–Η―¹–Μ–Β–Ϋ–Ϋ―΄―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è―Ö, –Α ―²–Α–Κ–Ε–Β –≤ –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Ψ–Ι –Ω―Ä–Α–Κ―²–Η–Κ–Β –Φ–Ϋ–Ψ–≥–Η―Ö –Ψ―³―²–Α–Μ―¨–Φ–Ψ–Μ–Ψ–≥–Ψ–≤ –≤ ―Ä–Α–Ζ–Ϋ―΄―Ö ―¹―²―Ä–Α–Ϋ–Α―Ö –Φ–Η―Ä–Α.
–î–Μ―è –Μ–Β―΅–Β–Ϋ–Η―è –Ϋ–Β―ç–Κ―¹―¹―É–¥–Α―²–Η–≤–Ϋ–Ψ–Ι ―³–Ψ―Ä–Φ―΄ –≤–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Ψ–Ι –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η–Η –Ω―Ä–Η–Φ–Β–Ϋ―è―é―²―¹―è –Ω―Ä–Β–Ω–Α―Ä–Α―²―΄, ―¹–Ψ–¥–Β―Ä–Ε–Α―â–Η–Β ―΅–Β―Ä–Ϋ–Η–Κ―É, –Α–Ϋ–≥–Η–Ψ–Ω―Ä–Ψ―²–Β–Κ―²–Ψ―Ä–Ϋ―΄–Β –Ω―Ä–Β–Ω–Α―Ä–Α―²―΄, ―¹―²–Α―²–Η–Ϋ―΄, ―¹–Ϋ–Η–Ε–Α―é―â–Η–Β ―É―Ä–Ψ–≤–Β–Ϋ―¨ ―Ö–Ψ–Μ–Β―¹―²–Β―Ä–Η–Ϋ–Α, –Η –Α–Ϋ―²–Η–Ψ–Κ―¹–Η–¥–Α–Ϋ―²―΄ [15-17]. –£―¹–Β ―ç―²–Η –Ω―Ä–Β–Ω–Α―Ä–Α―²―΄ –Ϋ–Α―Ö–Ψ–¥―è―² ―¹–≤–Ψ–Β –Ω―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η–Β –Η –≤ –Ω―Ä–Ψ―³–Η–Μ–Α–Κ―²–Η–Κ–Β ―Ä–Α–Ζ–≤–Η―²–Η―è –£–€–î.
–ö–Α–Κ ―É–Ε–Β ―É–Ω–Ψ–Φ–Η–Ϋ–Α–Μ–Ψ―¹―¨, –≤ –Ϋ–Α―¹―²–Ψ―è―â–Β–Β –≤―Ä–Β–Φ―è –≤–Β–¥–Β―²―¹―è –Α–Κ―²–Η–≤–Ϋ―΄–Ι –Ω–Ψ–Η―¹–Κ –Ϋ–Ψ–≤―΄―Ö –Ω–Ψ–¥―Ö–Ψ–¥–Ψ–≤ –Κ –Μ–Β―΅–Β–Ϋ–Η―é –≤–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Ψ–Ι –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η–Η. –ö–Α–Κ –Ω–Ψ–Κ–Α–Ζ–Α–Μ–Η –Φ–Ϋ–Ψ–≥–Ψ―΅–Η―¹–Μ–Β–Ϋ–Ϋ―΄–Β –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è, –Φ–Ψ–Μ–Β–Κ―É–Μ―΄, ―¹–Ψ―¹―²–Α–≤–Μ―è―é―â–Η–Β –Ψ―¹–Ϋ–Ψ–≤―É –Ω–Α―²–Ψ–≥–Β–Ϋ–Β–Ζ–Α –±–Ψ–Μ–Β–Ζ–Ϋ–Η, –Ω―Ä–Η–Ϋ–Η–Φ–Α―é―² ―É―΅–Α―¹―²–Η–Β –≤ –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ–Ψ–Φ ―Ü–Η–Κ–Μ–Β, –Φ–Β–Ε–Κ–Μ–Β―²–Ψ―΅–Ϋ―΄―Ö –≤–Ζ–Α–Η–Φ–Ψ–¥–Β–Ι―¹―²–≤–Η―è―Ö, –Ψ–Κ–Η―¹–Μ–Η―²–Β–Μ―¨–Ϋ―΄―Ö ―Ä–Β–Α–Κ―Ü–Η―è―Ö, ―è–≤–Μ―è―é―²―¹―è –Ψ―¹–Ϋ–Ψ–≤–Ψ–Ι –≤–Ϋ–Β–Κ–Μ–Β―²–Ψ―΅–Ϋ–Ψ–≥–Ψ –Φ–Α―²―Ä–Η–Κ―¹–Α. –≠―²–Η –Φ–Ψ–Μ–Β–Κ―É–Μ―΄ –Φ–Ψ–≥―É―² ―¹―²–Α―²―¨ –Ω–Ψ―²–Β–Ϋ―Ü–Η–Α–Μ―¨–Ϋ―΄–Φ–Η –Φ–Η―à–Β–Ϋ―è–Φ–Η ―²–Β―Ä–Α–Ω–Η–Η –£–€–î. –Δ–Α–Κ, –Η–Ζ―É―΅–Β–Ϋ–Η–Β –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ü–Η–Κ–Μ–Α –Ϋ–Α –Κ–Μ–Β―²–Ψ―΅–Ϋ–Ψ–Φ –Η –Φ–Ψ–Μ–Β–Κ―É–Μ―è―Ä–Ϋ–Ψ–Φ ―É―Ä–Ψ–≤–Ϋ–Β –Ψ―²–Κ―Ä―΄–≤–Α–Β―² ―¹–Ψ–≤―Ä–Β–Φ–Β–Ϋ–Ϋ–Ψ–Ι –Φ–Β–¥–Η―Ü–Η–Ϋ–Β –Ϋ–Ψ–≤―΄–Β –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Η―è –Ω–Ψ–Η―¹–Κ–Α –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤, –Ω―Ä–Β–Ω―è―²―¹―²–≤―É―é―â–Η―Ö –Ω―Ä–Ψ–≥―Ä–Β―¹―¹–Η―Ä–Ψ–≤–Α–Ϋ–Η―é –¥–Β–≥–Β–Ϋ–Β―Ä–Α―²–Η–≤–Ϋ―΄―Ö –Ω―Ä–Ψ―Ü–Β―¹―¹–Ψ–≤ –≤ ―¹―²―Ä―É–Κ―²―É―Ä–Α―Ö –≥–Μ–Α–Ζ–Α –Η, –≤ ―΅–Α―¹―²–Ϋ–Ψ―¹―²–Η, –≤ ―¹–Β―²―΅–Α―²–Κ–Β [18]. –Θ―΅―ë–Ϋ―΄–Φ–Η –≤―΄―è–≤–Μ–Β–Ϋ–Ψ, ―΅―²–Ψ –Φ―É―²–Α―Ü–Η―è –≥–Β–Ϋ–Α –Ω―Ä–Α–Κ―²–Η―΅–Β―¹–Κ–Η –Μ―é–±–Ψ–≥–Ψ ―É―΅–Α―¹―²–Ϋ–Η–Κ–Α –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –Κ–Α―¹–Κ–Α–¥–Α –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ –¥–Β–≥–Β–Ϋ–Β―Ä–Α―²–Η–≤–Ϋ―΄–Φ –Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η―è–Φ ―¹–Β―²―΅–Α―²–Κ–Η (–Ϋ–Α ―Ä–Η―¹―É–Ϋ–Κ–Β 2 –Ψ–±–Ψ–Ζ–Ϋ–Α―΅–Β–Ϋ―΄ –Φ―É―²–Α―Ü–Η–Η –Μ–Ψ–Κ―É―¹–Ψ–≤ –≥–Β–Ϋ–Ψ–≤, –Κ–Ψ–¥–Η―Ä―É―é―â–Η―Ö –±–Β–Μ–Κ–Η, –Ω―Ä–Η–Ϋ–Η–Φ–Α―é―â–Η–Β ―É―΅–Α―¹―²–Η–Β –≤ –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ–Ψ–Φ ―Ü–Η–Κ–Μ–Β [1]). –Γ–Μ–Β–¥–Ψ–≤–Α―²–Β–Μ―¨–Ϋ–Ψ, ―É―¹–Ω–Β―Ö –±–Ψ―Ä―¨–±―΄ ―¹ ―Ä–Α–Ζ–≤–Η―²–Η–Β–Φ –≤–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Ψ–Ι –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η–Η –≤–Ψ –Φ–Ϋ–Ψ–≥–Ψ–Φ –Ζ–Α–≤–Η―¹–Η―² –Ψ―² ―Ä–Α–Ζ–≤–Η―²–Η―è –¥―Ä―É–≥–Η―Ö –≤–Β―²–≤–Β–Ι –Φ–Β–¥–Η―Ü–Η–Ϋ―΄, –≤ ―΅–Α―¹―²–Ϋ–Ψ―¹―²–Η, –Ψ―²–Κ―Ä―΄―²–Η―è –≤ –Ψ–±–Μ–Α―¹―²–Η –≥–Β–Ϋ–Β―²–Η–Κ–Η –Φ–Ψ–≥―É―² –≤–Ϋ–Β―¹―²–Η –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ―΄–Ι –≤–Κ–Μ–Α–¥ –≤ ―Ä–Α–Ζ―Ä–Α–±–Ψ―²–Κ―É –Φ–Β―²–Ψ–¥–Ψ–≤ –Μ–Β―΅–Β–Ϋ–Η―è, –Η, ―΅―²–Ψ –Ϋ–Β –Φ–Β–Ϋ–Β–Β –≤–Α–Ε–Ϋ–Ψ, –Ω―É―²–Β–Ι –Ω―Ä–Ψ―³–Η–Μ–Α–Κ―²–Η–Κ–Η –£–€–î.
–£ –Ϋ–Α―¹―²–Ψ―è―â–Β–Β –≤―Ä–Β–Φ―è –Ψ―¹―É―â–Β―¹―²–≤–Μ―è–Β―²―¹―è –Α–Κ―²–Η–≤–Ϋ―΄–Ι –Ω–Ψ–Η―¹–Κ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ (–Α–Ϋ―²–Α–≥–Ψ–Ϋ–Η―¹―²–Ψ–≤, –±–Μ–Ψ–Κ–Α―²–Ψ―Ä–Ψ–≤, –Α–Κ―²–Η–≤–Α―²–Ψ―Ä–Ψ–≤ –±–Β–Μ–Κ–Ψ–≤, ―É―΅–Α―¹―²–≤―É―é―â–Η―Ö –≤ –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ–Ψ–Φ ―Ü–Η–Κ–Μ–Β), –Ω―Ä–Β–Ω―è―²―¹―²–≤―É―é―â–Η―Ö –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η―é, –Μ–Η–±–Ψ ―²–Ψ―Ä–Φ–Ψ–Ζ―è―â–Η―Ö –Ϋ–Α–Κ–Ψ–Ω–Μ–Β–Ϋ–Η–Β ―²–Ψ–Κ―¹–Η―΅–Ϋ–Ψ–≥–Ψ –ê2–ï, –Α, ―¹–Μ–Β–¥–Ψ–≤–Α―²–Β–Μ―¨–Ϋ–Ψ, ―¹–Ϋ–Η–Ε–Α―é―â–Η―Ö ―Ä–Η―¹–Κ –Ϋ–Α―¹―²―É–Ω–Μ–Β–Ϋ–Η―è ―¹–Μ–Β–Ω–Ψ―²―΄ (―Ä–Η―¹. 3) [19, 20]. –£ ―΅–Α―¹―²–Ϋ–Ψ―¹―²–Η, –Α–Κ―²–Η–≤–Ϋ–Ψ –Η―¹―¹–Μ–Β–¥―É―é―²―¹―è –Α–Ϋ―²–Α–≥–Ψ–Ϋ–Η―¹―²―΄ –±–Β–Μ–Κ–Α Rpe65 βÄ™ –≤–Α–Ε–Ϋ–Ψ–≥–Ψ ―É―΅–Α―¹―²–Ϋ–Η–Κ–Α –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ü–Η–Κ–Μ–Α. –®–Α–Ω–Β―Ä–Ψ–Ϋ Rpe65 –Ζ–Α–Ϋ–Η–Φ–Α–Β―² ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ–Ψ–Β –Φ–Β―¹―²–Ψ –≤ ―¹–Μ–Ψ–Ε–Ϋ–Ψ–Φ –Α–Ϋ―¹–Α–Φ–±–Μ–Β –±–Β–Μ–Κ–Ψ–≤ βÄ™ –Φ―É–Μ―¨―²–Η―³–Β―Ä–Φ–Β–Ϋ―²–Ϋ–Ψ–Φ –Κ–Ψ–Φ–Ω–Μ–Β–Κ―¹–Β, ―³―É–Ϋ–Κ―Ü–Η–Ψ–Ϋ–Η―Ä―É―é―â–Β–Φ –≤ –Κ–Μ–Β―²–Κ–Α―Ö –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è. –Λ―É–Ϋ–Κ―Ü–Η―è Rpe65 ―¹–Ψ―¹―²–Ψ–Η―² –≤ –Η–Ζ–≤–Μ–Β―΅–Β–Ϋ–Η–Η –Ϋ–Β―Ä–Α―¹―²–≤–Ψ―Ä–Η–Φ―΄―Ö ―²―Ä–Α–Ϋ―¹-―Ä–Β―²–Η–Ϋ–Η–Μ–Ψ–≤―΄―Ö ―ç―³–Η―Ä–Ψ–≤ –Η–Ζ –Φ–Β–Φ–±―Ä–Α–Ϋ―΄ –Η –Ω―Ä–Β–¥―¹―²–Α–≤–Μ–Β–Ϋ–Η–Η –Η―Ö –Η–Ζ–Ψ–Φ–Β―Ä–Ψ–≥–Η–¥―Ä–Ψ–Μ–Α–Ζ–Β, –Κ–Ψ―²–Ψ―Ä–Α―è, –≤ ―¹–≤–Ψ―é –Ψ―΅–Β―Ä–Β–¥―¨, –Η―¹–Ω–Ψ–Μ―¨–Ζ―É―è ―ç–Ϋ–Β―Ä–≥–Η―é –≥–Η–¥―Ä–Ψ–Μ–Η–Ζ–Α ―²―Ä–Α–Ϋ―¹-―Ä–Β―²–Η–Ϋ–Η–Μ–Ψ–≤―΄―Ö ―ç―³–Η―Ä–Ψ–≤, –Ω―Ä–Β–≤―Ä–Α―â–Α–Β―² –Η―Ö –≤ 11-―Ü–Η―¹-―Ä–Β―²–Η–Ϋ–Ψ–Μ. Rpe65 –≤ –Ϋ–Α―¹―²–Ψ―è―â–Β–Β –≤―Ä–Β–Φ―è ―Ä–Α―¹―¹–Φ–Α―²―Ä–Η–≤–Α–Β―²―¹―è –Κ–Α–Κ –Φ–Η―à–Β–Ϋ―¨ –Μ–Β–Κ–Α―Ä―¹―²–≤–Β–Ϋ–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Η –Ω―Ä–Η –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η–Η. –Γ―É―â–Β―¹―²–≤―É–Β―² ―Ü–Β–Μ–Α―è –Η–Ϋ–¥―É―¹―²―Ä–Η―è –Ω–Ψ –Ω–Ψ–Η―¹–Κ―É –Α–Ϋ―²–Α–≥–Ψ–Ϋ–Η―¹―²–Ψ–≤ Rpe65. –£ –Κ–Α―΅–Β―¹―²–≤–Β ―²–Α–Κ–Η―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ –Ω―Ä–Β–¥–Μ–Α–≥–Α―é―²―¹―è ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Β ―Ä–Β―²–Η–Ϋ–Ψ–Η–¥―΄: –Ϋ–Α–Ω―Ä–Η–Φ–Β―Ä, –Η–Ζ–Ψ―²―Ä–Β―²–Η–Ϋ–Ψ–Η–Ϋ (13-―Ü–Η―¹-―Ä–Β―²–Η–Ϋ–Ψ–Η–¥–Ϋ–Α―è –Κ–Η―¹–Μ–Ψ―²–Α) –Η –Β–≥–Ψ –Φ–Ψ–¥–Η―³–Η–Κ–Α―Ü–Η–Η. –‰–Ζ–Ψ―²―Ä–Β―²–Η–Ϋ–Ψ–Η–Ϋ ―΅–Α―¹―²–Η―΅–Ϋ–Ψ –±–Μ–Ψ–Κ–Η―Ä―É–Β―² –¥–Β–Ι―¹―²–≤–Η–Β Rpe65, ―΅―²–Ψ ―¹–Ϋ–Η–Ε–Α–Β―² ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ü–Η–Κ–Μ–Α –Η, –Κ–Α–Κ ―¹–Μ–Β–¥―¹―²–≤–Η–Β, ―É–Φ–Β–Ϋ―¨―à–Α–Β―² –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η–Β ―²–Ψ–Κ―¹–Η―΅–Ϋ–Ψ–≥–Ψ –ê2–ï [21, 22].
–‰–Ϋ–Ψ–Ι –Φ–Η―à–Β–Ϋ―¨―é –≤ –Μ–Β―΅–Β–Ϋ–Η–Η –£–€–î, –Ω–Ψ–Ζ–≤–Ψ–Μ―è―é―â–Β–Ι ―¹–Ϋ–Η–Ζ–Η―²―¨ –Ω―Ä–Ψ–≥―Ä–Β―¹―¹–Η―é –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è, ―è–≤–Μ―è―é―²―¹―è –±–Β–Μ–Κ–Η ―³–Η–±―É–Μ–Η–Ϋ―΄. –î–Ψ–Κ–Α–Ζ–Α–Ϋ–Ψ, ―΅―²–Ψ ―ç―²–Η –±–Β–Μ–Κ–Η ―è–≤–Μ―è―é―²―¹―è –Ψ–¥–Ϋ–Η–Φ –Η–Ζ –≤–Α–Ε–Ϋ–Β–Ι―à–Η―Ö –Κ–Ψ–Φ–Ω–Ψ–Ϋ–Β–Ϋ―²–Ψ–≤, –Φ–Ψ–¥―É–Μ–Η―Ä―É―é―â–Η–Φ ―³―É–Ϋ–Κ―Ü–Η―é –Φ–Β–Φ–±―Ä–Α–Ϋ―΄ –ë―Ä―É―Ö–Α, –Κ–Ψ―²–Ψ―Ä–Α―è –Ω―Ä–Β―²–Β―Ä–Ω–Β–≤–Α–Β―² –Ω–Α―²–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Β –Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η―è –Ω―Ä–Η –£–€–î. –ù–Α –Ψ―¹–Ϋ–Ψ–≤–Β ―ç―²–Η―Ö –±–Β–Μ–Κ–Ψ–≤, ―è–≤–Μ―è―é―â–Η―Ö―¹―è ―à–Α–Ω–Β―Ä–Ψ–Ϋ–Α–Φ–Η –Φ–Β–Ε–Κ–Μ–Β―²–Ψ―΅–Ϋ–Ψ–≥–Ψ –Φ–Α―²―Ä–Η–Κ―¹–Α, –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ ―¹–Ψ–Ζ–¥–Α–Ϋ–Η–Β –Μ–Β–Κ–Α―Ä―¹―²–≤, –≥–¥–Β ―³–Η–±―É–Μ–Η–Ϋ―΄ –±―É–¥―É―² –≤―΄―¹―²―É–Ω–Α―²―¨ –≤ –Κ–Α―΅–Β―¹―²–≤–Β ―¹―²–Α–±–Η–Μ–Η–Ζ–Α―²–Ψ―Ä–Ψ–≤ –Φ–Β–Ε–Κ–Μ–Β―²–Ψ―΅–Ϋ–Ψ–≥–Ψ –Φ–Α―²―Ä–Η–Κ―¹–Α, –Α –≤ ―΅–Α―¹―²–Ϋ–Ψ―¹―²–Η –Φ–Β–Φ–±―Ä–Α–Ϋ―΄ –ë―Ä―É―Ö–Α. –ù–Β–¥–Α–≤–Ϋ–Β–Β –Ψ―²–Κ―Ä―΄―²–Η–Β ―³–Η–±―É–Μ–Η–Ϋ–Ψ–≤ –Ω–Ψ–Ζ–≤–Ψ–Μ–Η–Μ–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α―²–Β–Μ―è–Φ –Φ–Ψ–Μ–Β–Κ―É–Μ―è―Ä–Ϋ―΄―Ö –Ψ―¹–Ϋ–Ψ–≤ –Ζ―Ä–Β–Ϋ–Η―è –Ω―Ä–Β–¥–Ω–Ψ–Μ–Ψ–Ε–Η―²―¨, ―΅―²–Ψ –Η―Ö –¥–Β―³–Β–Κ―² –Φ–Ψ–Ε–Β―² –±―΄―²―¨ –Ψ–¥–Ϋ–Ψ–Ι –Η–Ζ –Ω―Ä–Η―΅–Η–Ϋ –£–€–î (―Ä–Η―¹. 4). –Δ–Α–Κ, –Ϋ–Α–Ω―Ä–Η–Φ–Β―Ä, –Φ―É―²–Α―Ü–Η–Η ―³–Η–±―É–Μ–Η–Ϋ–Α 5, –Ϋ–Α―Ö–Ψ–¥―è―â–Β–≥–Ψ―¹―è –≤ –Φ–Β–Φ–±―Ä–Α–Ϋ–Β –ë―Ä―É―Ö–Α –Η ―É―΅–Α―¹―²–≤―É―é―â–Β–≥–Ψ –≤ ―³–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Ϋ–Η–Η –Η –Ψ―Ä–≥–Α–Ϋ–Η–Ζ–Α―Ü–Η–Η ―ç–Μ–Α―¹―²–Η―΅–Β―¹–Κ–Η―Ö –≤–Ψ–Μ–Ψ–Κ–Ψ–Ϋ, –≤–Β–¥―É―² –Κ –Ϋ–Α―Ä―É―à–Β–Ϋ–Η―é –Β–Β ―³―É–Ϋ–Κ―Ü–Η–Η –Η, –Κ–Α–Κ ―¹–Μ–Β–¥―¹―²–≤–Η–Β, –Ϋ–Α―Ä―É―à–Β–Ϋ–Η―é ―³–Α–≥–Ψ―Ü–Η―²–Α―Ä–Ϋ–Ψ–Ι –Η –Μ–Η–Ζ–Η―¹–Ϋ–Ψ–Ι ―¹–Ω–Ψ―¹–Ψ–±–Ϋ–Ψ―¹―²–Η ―Ä–Β―²–Η–Ϋ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è. –≠―²–Ψ―² –Ω―Ä–Ψ―Ü–Β―¹―¹ –Ζ–Α–Κ–Α–Ϋ―΅–Η–≤–Α–Β―²―¹―è –Ϋ–Α–Κ–Ψ–Ω–Μ–Β–Ϋ–Η–Β–Φ –Μ–Η–Ω–Ψ―³―É―¹―Ü–Η–Ϋ–Α, –≤–Β–¥―É―â–Β–≥–Ψ –Κ –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η―é –¥―Ä―É–Ζ [23]. –£–Ω–Ψ―¹–Μ–Β–¥―¹―²–≤–Η–Η ―É–≤–Β–Μ–Η―΅–Η–≤–Α―é―â–Η–Β―¹―è –≤ ―Ä–Α–Ζ–Φ–Β―Ä–Α―Ö –¥―Ä―É–Ζ―΄ –Ω―Ä–Η–≤–Ψ–¥―è―² –Κ –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η―é –¥–Β―³–Β–Κ―²–Ψ–≤ –≤ –Φ–Β–Φ–±―Ä–Α–Ϋ–Β –ë―Ä―É―Ö–Α –Η –Α―²―Ä–Ψ―³–Η–Η –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è. –ß–Β―Ä–Β–Ζ –¥–Β―³–Β–Κ―²―΄ –≤ –Φ–Β–Φ–±―Ä–Α–Ϋ–Β –ë―Ä―É―Ö–Α ―ç–Κ―¹―¹―É–¥–Α―², –Ψ–±―Ä–Α–Ζ―É―é―â–Η–Ι―¹―è –≤ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Β –Ω–Ψ–≤―΄―à–Β–Ϋ–Ϋ–Ψ–Ι –Ω―Ä–Ψ–Ϋ–Η―Ü–Α–Β–Φ–Ψ―¹―²–Η ―¹–Ψ―¹―É–¥–Ψ–≤ ―Ö–Ψ―Ä–Η–Ψ–Κ–Α–Ω–Η–Μ–Μ―è―Ä–Ϋ–Ψ–≥–Ψ ―¹–Μ–Ψ―è, –Ω―Ä–Ψ–Ϋ–Η–Κ–Α–Β―² –Ω–Ψ–¥ –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ―΄–Ι ―ç–Ω–Η―²–Β–Μ–Η–Ι, –Ω―Ä–Η–≤–Ψ–¥―è –Κ ―ç–Κ―¹―¹―É–¥–Α―²–Η–≤–Ϋ–Ψ–Ι –Ψ―²―¹–Μ–Ψ–Ι–Κ–Β –Ω–Ψ―¹–Μ–Β–¥–Ϋ–Β–≥–Ψ, –≤―΄–Ζ―΄–≤–Α―è –Ψ―²–Β–Κ –Η –≥–Η–Ω–Ψ–Κ―¹–Η―é ―Ä–Β―²–Η–Ϋ–Α–Μ―¨–Ϋ–Ψ–Ι ―²–Κ–Α–Ϋ–Η. –Δ–Α–Κ ―Ä―è–¥ ―ç―²–Η―Ö ―³–Α–Κ―²–Ψ―Ä–Ψ–≤ ―¹–Ω–Ψ―¹–Ψ–±―¹―²–≤―É–Β―² ―Ä–Α–Ζ–≤–Η―²–Η―é –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η–Η ―¹–Β―²―΅–Α―²–Κ–Η.
–î―Ä―É–≥–Η–Φ –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Η–Β–Φ –Ω–Ψ–Η―¹–Κ–Α ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è –£–€–î ―è–≤–Μ―è–Β―²―¹―è –Η–Ζ―É―΅–Β–Ϋ–Η–Β ―¹–≤–Ψ–Ι―¹―²–≤ –Φ–Ϋ–Ψ–≥–Ψ―³―É–Ϋ–Κ―Ü–Η–Ψ–Ϋ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –±–Β–Μ–Κ–Α ―ç―Ä–Η―²―Ä–Ψ–Ω–Ψ―ç―²–Η–Ϋ–Α, ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä―΄ –Κ –Κ–Ψ―²–Ψ―Ä–Ψ–Φ―É –Η–Φ–Β―é―²―¹―è –Ϋ–Α –≤–Ϋ―É―²―Ä–Β–Ϋ–Ϋ–Β–Φ ―¹–Β–≥–Φ–Β–Ϋ―²–Β ―³–Ψ―²–Ψ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Α. –ë―΄–Μ–Ψ –Ζ–Α–Φ–Β―΅–Β–Ϋ–Ψ, ―΅―²–Ψ –Ϋ–Β–Ι―Ä–Ψ–Ϋ―΄ ―¹–Β―²―΅–Α―²–Κ–Η, –Ω–Β―Ä–Β–Ϋ–Β―¹―à–Η–Β –≥–Η–Ω–Ψ–Κ―¹–Η―é, –±–Ψ–Μ–Β–Β ―É―¹―²–Ψ–Ι―΅–Η–≤―΄ –Κ –Η–Ζ–±―΄―²–Ψ―΅–Ϋ–Ψ–Φ―É –¥–Β–Ι―¹―²–≤–Η―é ―¹–≤–Β―²–Α –≤―¹–Μ–Β–¥―¹―²–≤–Η–Β ―²–Ψ―Ä–Φ–Ψ–Ε–Β–Ϋ–Η―è –Α–Ω–Ψ–Ω―²–Ψ–Ζ–Α. –™–Η–Ω–Ψ–Κ―¹–Η―è –≤―΄–Ζ―΄–≤–Α–Β―² ―¹―²–Α–±–Η–Μ–Η–Ζ–Α―Ü–Η―é –≥–Η–Ω–Ψ–Κ―¹–Η―è-–Η–Ϋ–¥―É―Ü–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–≥–Ψ ―³–Α–Κ―²–Ψ―Ä–Α-1 (hypoxia-induced factor HIF-1), –Κ–Ψ―²–Ψ―Ä―΄–Ι ―è–≤–Μ―è–Β―²―¹―è ―²―Ä–Α–Ϋ―¹–Κ―Ä–Η–Ω―Ü–Η–Ψ–Ϋ–Ϋ―΄–Φ ―³–Α–Κ―²–Ψ―Ä–Ψ–Φ –¥–Μ―è ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄―Ö –≥–Β–Ϋ–Ψ–≤, –Κ–Ψ–¥–Η―Ä―É―é―â–Η―Ö –±–Β–Μ–Κ–Η, –Ω–Ψ–≤―΄―à–Α―é―â–Η–Β –Α–¥–Α–Ω―²–Α―Ü–Η―é ―²–Κ–Α–Ϋ–Β–Ι –Κ –≥–Η–Ω–Ψ–Κ―¹–Η–Η. –Δ–Α–Κ–Η–Φ–Η –±–Β–Μ–Κ–Α–Φ–Η ―è–≤–Μ―è―é―²―¹―è VEGF –Η ―ç―Ä–Η―²―Ä–Ψ–Ω–Ψ―ç―²–Η–Ϋ. –‰–Φ–Β–Ϋ–Ϋ–Ψ –Ω–Ψ―¹–Μ–Β–¥–Ϋ–Η–Ι –±–Β–Μ–Ψ–Κ, –Α–Κ―²–Η–≤–Η―Ä―É―è ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä ―ç―Ä–Η―²―Ä–Ψ–Ω–Ψ―ç―²–Η–Ϋ–Α ―³–Ψ―²–Ψ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ϋ–Ψ–Ι –Κ–Μ–Β―²–Κ–Η, –Η–Ϋ–≥–Η–±–Η―Ä―É–Β―² –Α–Ω–Ψ–Ω―²–Ψ–Ζ –Ϋ–Β–Ι―Ä–Ψ–Ϋ–Α - –Ω―Ä–Ψ―Ü–Β―¹―¹, –Κ–Ψ―²–Ψ―Ä―΄–Ι, –Κ–Α–Κ –Η–Ζ–≤–Β―¹―²–Ϋ–Ψ, ―è–≤–Μ―è–Β―²―¹―è –Ψ–¥–Ϋ–Ψ–Ι –Η–Ζ –Ω―Ä–Η―΅–Η–Ϋ –Ω–Ψ―²–Β―Ä–Η –Ζ―Ä–Β–Ϋ–Η―è –Ω―Ä–Η –£–€–î. –≠―Ä–Η―²―Ä–Ψ–Ω–Ψ―ç―²–Η–Ϋ, –Ω–Ψ–Φ–Η–Φ–Ψ –Ϋ–Β–Ι―Ä–Ψ–Ω―Ä–Ψ―²–Β–Κ―²–Ψ―Ä–Ϋ–Ψ–≥–Ψ –¥–Β–Ι―¹―²–≤–Η―è (–Ω―Ä–Β–¥–Ψ―²–≤―Ä–Α―â–Β–Ϋ–Η―è –Α–Ω–Ψ–Ω―²–Ψ–Ζ–Α) –Ψ–±–Μ–Α–¥–Α–Β―² –Η –¥―Ä―É–≥–Η–Φ–Η ―ç―³―³–Β–Κ―²–Α–Φ–Η: ―¹―²–Η–Φ―É–Μ―è―Ü–Η–Β–Ι ―ç―Ä–Η―²―Ä–Ψ–Ω–Ψ―ç–Ζ–Α –Η –Α–Ϋ–≥–Η–Ψ–≥–Β–Ϋ–Β–Ζ–Α. –ü–Ψ―ç―²–Ψ–Φ―É –≤―΄–¥–Β–Μ–Β–Ϋ–Η–Β ―΅–Α―¹―²–Η –±–Β–Μ–Κ–Ψ–≤–Ψ–Ι –Φ–Ψ–Μ–Β–Κ―É–Μ―΄ ―ç―Ä–Η―²―Ä–Ψ–Ω–Ψ―ç―²–Η–Ϋ–Α, –Ψ–Ω―Ä–Β–¥–Β–Μ―è―é―â–Β–Ι ―²–Ψ–Μ―¨–Κ–Ψ –Ϋ–Β–Ι―Ä–Ψ–Ω―Ä–Ψ―²–Β–Κ―²–Η–≤–Ϋ–Ψ–Β –¥–Β–Ι―¹―²–≤–Η–Β, –Η–Μ–Η ―¹–Η–Ϋ―²–Β–Ζ –Ω–Ψ–Μ–Η–Ω–Β–Ω―²–Η–¥–Α, –Ψ–±–Μ–Α–¥–Α―é―â–Β–≥–Ψ –Ω–Ψ–¥–Ψ–±–Ϋ―΄–Φ–Η ―ç―Ä–Η―²―Ä–Ψ–Ω–Ψ―ç―²–Η–Ϋ―É ―¹–≤–Ψ–Ι―¹―²–≤–Α–Φ–Η –≤ –Ψ―²–Ϋ–Ψ―à–Β–Ϋ–Η–Η –Α–Ω–Ψ–Ω―²–Ψ–Ζ–Α ―³–Ψ―²–Ψ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤, –Ω–Ψ–Ζ–≤–Ψ–Μ–Η―² –Ω―Ä–Β–¥–Ψ―²–≤―Ä–Α―²–Η―²―¨ –Φ–Ϋ–Ψ–≥–Ψ―΅–Η―¹–Μ–Β–Ϋ–Ϋ―΄–Β –Ω–Ψ–±–Ψ―΅–Ϋ―΄–Β ―ç―³―³–Β–Κ―²―΄. [24].
–ü–Β―Ä―¹–Ω–Β–Κ―²–Η–≤–Ϋ―΄–Φ –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Η–Β–Φ –≤ –Μ–Β―΅–Β–Ϋ–Η–Η –£–€–î ―è–≤–Μ―è–Β―²―¹―è ―²–Α–Κ–Ε–Β –Ω–Ψ–Η―¹–Κ –Α–≥–Ψ–Ϋ–Η―¹―²–Ψ–≤ ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤ –Α–Κ―²–Η–≤–Α―Ü–Η–Η –Ω–Β―Ä–Ψ–Κ―¹–Η―¹–Ψ–Φ, –Η–Μ–Η PPAR (peroxisome proliferator-activated receptors). –û–Ϋ–Η –Ψ–±–Μ–Α–¥–Α―é―² –Ω―Ä–Ψ―²–Η–≤–Ψ–≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ―΄–Φ –Η –Ϋ–Β–Ι―Ä–Ψ–Ω―Ä–Ψ―²–Β–Κ―²–Ψ―Ä–Ϋ―΄–Φ –¥–Β–Ι―¹―²–≤–Η–Β–Φ, –Ω―Ä–Η–Ϋ–Η–Φ–Α―é―² ―É―΅–Α―¹―²–Η–Β –≤–Ψ –Φ–Ϋ–Ψ–≥–Η―Ö –Φ–Β―²–Α–±–Ψ–Μ–Η―΅–Β―¹–Κ–Η―Ö ―Ü–Β–Ω–Ψ―΅–Κ–Α―Ö, –≤ ―²–Ψ–Φ ―΅–Η―¹–Μ–Β –Η –≤ ―²–Β―Ö, –Κ–Ψ―²–Ψ―Ä―΄–Β ―¹–Ψ―¹―²–Α–≤–Μ―è―é―² –Ψ―¹–Ϋ–Ψ–≤―É –Ω–Α―²–Ψ–≥–Β–Ϋ–Β–Ζ–Α –£–€–î: –Ψ–±–Φ–Β–Ϋ–Β –Μ–Η–Ω–Η–¥–Ψ–≤, –Α–Ϋ―²–Η–Ψ–Κ―¹–Η–¥–Α–Ϋ―²–Ϋ–Ψ–Ι –Ζ–Α―â–Η―²–Β, ―Ä–Β–≥―É–Μ―è―Ü–Η–Η –Η–Φ–Φ―É–Ϋ–Ϋ–Ψ–≥–Ψ –Ψ―²–≤–Β―²–Α, ―Ä–Β–Α–Μ–Η–Ζ–Α―Ü–Η–Η –¥–Β–Ι―¹―²–≤–Η―è VEGF –Η ―ç–Κ―¹–Ω―Ä–Β―¹―¹–Η–Η –≥–Β–Ϋ–Ψ–≤ –Φ–Α―²―Ä–Η–Κ―¹–Ϋ―΄―Ö –Φ–Β―²–Α–Μ–Μ–Ψ–Ω―Ä–Ψ―²–Β–Η–Ϋ–Α–Ζ (―Ä–Η―¹.5). –‰–Ζ–≤–Β―¹―²–Ϋ―΄ 3 –Η–Ζ–Ψ―³–Ψ―Ä–Φ―΄ PPAR: ?, ? –Η ?. –‰–Ζ–Ψ―³–Ψ―Ä–Φ―΄ ? –Η ? –Ϋ–Α–Ι–¥–Β–Ϋ―΄ –≤ –Κ–Μ–Β―²–Κ–Α―Ö ―¹–Β―²―΅–Α―²–Κ–Η, –Φ–Ψ–Ϋ–Ψ―Ü–Η―²–Α―Ö –Η –Φ–Α–Κ―Ä–Ψ―³–Α–≥–Α―Ö, –Ω―Ä–Η–Ϋ–Η–Φ–Α―é―â–Η―Ö ―É―΅–Α―¹―²–Η–Β –≤ ―Ä–Α–Ζ–≤–Η―²–Η–Η –£–€–î. –ê–≥–Ψ–Ϋ–Η―¹―²–Α–Φ–Η PPAR? –Η PPAR? ―è–≤–Μ―è―é―²―¹―è ―³–Β–Ϋ–Ψ―³–Η–±―Ä–Α―² –Η ―²–Η–Ψ–Ζ–Ψ–Μ–Η–¥–Η–Ϋ–¥–Η–Ψ–Ϋ (―²―Ä–Ψ–≥–Μ–Η―²–Α–Ζ–Ψ–Ϋ) ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ, ―²–Α–Κ–Ε–Β ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä―΄ –Α–Κ―²–Η–≤–Α―Ü–Η–Η –Ω–Β―Ä–Ψ–Κ―¹–Η―¹–Ψ–Φ –Φ–Ψ–≥―É―² –≤–Ζ–Α–Η–Φ–Ψ–¥–Β–Ι―¹―²–≤–Ψ–≤–Α―²―¨ ―¹ –¥―Ä―É–≥–Η–Φ–Η –≤–Β―â–Β―¹―²–≤–Α–Φ–Η –Μ–Η–Ω–Η–¥–Ϋ–Ψ–Ι –Ω―Ä–Η―Ä–Ψ–¥―΄ [25, 26]. –û―΅–Β–≤–Η–¥–Ϋ–Ψ, ―΅―²–Ψ –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ―΄ –¥–Α–Μ―¨–Ϋ–Β–Ι―à–Η–Β –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è ―Ä–Ψ–Μ–Η –≤–Α–Ε–Ϋ―΄―Ö –Φ–Β―²–Α–±–Ψ–Μ–Η―΅–Β―¹–Κ–Η―Ö ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤ PPAR –≤ ―¹–Β―²―΅–Α―²–Κ–Β, –Η―Ö –≤–Μ–Η―è–Ϋ–Η―è –Ϋ–Α ―ç–Κ―¹–Ω―Ä–Β―¹―¹–Η―é –≥–Β–Ϋ–Ψ–≤ –Ω―Ä–Η –£–€–î. –†–Α―¹―à–Η―Ä–Β–Ϋ–Η–Β –Ζ–Ϋ–Α–Ϋ–Η–Ι –Ψ ―è–¥–Β―Ä–Ϋ―΄―Ö ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Α―Ö PPAR –Ω–Ψ–Ζ–≤–Ψ–Μ–Η―² –Ϋ–Α–Ι―²–Η –Ω―É―²–Η –≤–Ψ–Ζ–¥–Β–Ι―¹―²–≤–Η―è –Ϋ–Α ―³―É–Ϋ–Κ―Ü–Η―é ―Ä–Α–Ζ–Ϋ―΄―Ö ―³–Ψ―Ä–Φ –¥–Α–Ϋ–Ϋ―΄―Ö ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤ –Η ―¹–¥–Β–Μ–Α―²―¨ –Μ–Β―΅–Β–Ϋ–Η–Β –±–Ψ–Μ–Β–Β –Η–Ζ–±–Η―Ä–Α―²–Β–Μ―¨–Ϋ―΄–Φ.
–ü–Ψ―¹–Κ–Ψ–Μ―¨–Κ―É –¥–Ψ–Κ–Α–Ζ–Α–Ϋ–Ψ, ―΅―²–Ψ –≤ ―Ä–Α–Ζ–≤–Η―²–Η–Η –£–€–î –≤–Α–Ε–Ϋ–Α―è ―Ä–Ψ–Μ―¨ –Ω―Ä–Η–Ϋ–Α–¥–Μ–Β–Ε–Η―² –≥–Β–Ϋ–Β―²–Η―΅–Β―¹–Κ–Η–Φ ―³–Α–Κ―²–Ψ―Ä–Α–Φ, –≤ –±―É–¥―É―â–Β–Φ –±–Ψ–Μ―¨―à–Ψ–Ι –≤–Κ–Μ–Α–¥ –≤ ―Ä–Α–Ζ–≤–Η―²–Η–Β –Φ–Β―²–Ψ–¥–Ψ–≤ –Μ–Β―΅–Β–Ϋ–Η―è –£–€–î –≤–Ϋ–Β―¹―É―² –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –≥–Β–Ϋ–Ψ–Φ–Α –Κ–Α–Ε–¥–Ψ–≥–Ψ –Κ–Ψ–Ϋ–Κ―Ä–Β―²–Ϋ–Ψ–≥–Ψ –Ω–Α―Ü–Η–Β–Ϋ―²–Α, –Κ–Ψ―²–Ψ―Ä―΄–Β –Ω–Ψ–Ζ–≤–Ψ–Μ―è―² –Ψ―²–Ϋ–Ψ―¹–Η―²―¨ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Κ –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Ϋ―΄–Φ –≥―Ä―É–Ω–Ω–Α–Φ ―Ä–Η―¹–Κ–Α ―Ä–Α–Ζ–≤–Η―²–Η―è –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Η. –™–Β–Ϋ–Β―²–Η―΅–Β―¹–Κ–Η–Β ―²–Β―¹―²―΄ –Ω–Ψ–Ζ–≤–Ψ–Μ―è―² –≤―Ä–Α―΅―É –Ψ―¹―É―â–Β―¹―²–≤–Μ―è―²―¨ ―Ä–Α–Ϋ–Ϋ―é―é ―ç―³―³–Β–Κ―²–Η–≤–Ϋ―É―é –Ω―Ä–Ψ―³–Η–Μ–Α–Κ―²–Η–Κ―É –Η –Ω–Ψ–¥–±–Η―Ä–Α―²―¨ –Η–Ϋ–¥–Η–≤–Η–¥―É–Α–Μ―¨–Ϋ―΄–Β ―¹―Ö–Β–Φ―΄ –Μ–Β―΅–Β–Ϋ–Η―è [1].
–£ –¥–Α–Ϋ–Ϋ–Ψ–Ι ―Ä–Α–±–Ψ―²–Β –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ―΄ –Ϋ–Α―É―΅–Ϋ―΄–Β –Ω―Ä–Ψ–Β–Κ―²―΄ –Α–≤―²–Ψ―Ä–Ψ–≤ βÄ™ –≤―΄–Ω―É―¹–Κ–Ϋ–Η–Κ–Ψ–≤ –ë–Η–Ψ―Ö–Η–Φ–Η―΅–Β―¹–Κ–Ψ–Ι –®–Κ–Ψ–Μ―΄ –≠―¹―¹–Β–Η―¹―²–Ψ–≤ –Κ–Α―³–Β–¥―Ä―΄ –±–Η–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–Ι ―Ö–Η–Φ–Η–Η –€–€–ê –Η–Φ. –‰.–€. –Γ–Β―΅–Β–Ϋ–Ψ–≤–Α:
- –ë–Ψ–Μ–±–Α―¹ –½–Ψ–Η –£–Α―¹–Η–Μ―¨–Β–≤–Ϋ―΄ ¬Ϊ–£–Μ–Η―è–Ϋ–Η–Β –±–Β–Μ–Κ–Ψ–≤ –Φ–Β–Ε–Κ–Μ–Β―²–Ψ―΅–Ϋ–Ψ–≥–Ψ –Φ–Α―²―Ä–Η–Κ―¹–Α –Ϋ–Α ―Ä–Α–Ζ–≤–Η―²–Η–Β –≤–Ψ–Ζ―Ä–Α―¹―²–Ϋ―΄―Ö –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η–Ι –≥–Μ–Α–Ζ–Α¬Μ, 2006 –≥–Ψ–¥
- –£–Α―¹–Η–Μ–Β–≤―¹–Κ–Ψ–Ι –ù–Α―²–Α–Μ―¨–Η –ê–Ϋ–Α―²–Ψ–Μ―¨–Β–≤–Ϋ―΄ ¬Ϊ–£–Ζ–Α–Η–Φ–Ψ–¥–Β–Ι―¹―²–≤–Η–Β –Φ–Ψ–Μ–Β–Κ―É–Μ –Η –Κ–Μ–Β―²–Ψ–Κ –≤ –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ–Ψ–Φ ―Ü–Η–Κ–Μ–Β: ―à–Α–Ω–Β―Ä–Ψ–Ϋ RPE65 –Κ–Α–Κ –Φ–Η―à–Β–Ϋ―¨ –Μ–Β–Κ–Α―Ä―¹―²–≤–Β–Ϋ–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Η –Ω―Ä–Η –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η–Η¬Μ, 2006.
- –ß–Η–Κ―É–Ϋ –ï–Κ–Α―²–Β―Ä–Η–Ϋ―΄ –ê–Ϋ–Α―²–Ψ–Μ―¨–Β–≤–Ϋ―΄ ¬Ϊ–ù–Β–Κ–Ψ―²–Ψ―Ä―΄–Β –Φ–Ψ–Μ–Β–Κ―É–Μ―è―Ä–Ϋ―΄–Β –Α―¹–Ω–Β–Κ―²―΄ –Ϋ–Β–Ψ–≤–Α―¹–Κ―É–Μ―è―Ä–Η–Ζ–Α―Ü–Η–Η –Ω―Ä–Η –≤–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Ψ–Ι –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η–Η¬Μ, 2008.
–‰–Μ–Μ―é―¹―²―Ä–Α―Ü–Η–Η:
–†–Η―¹. 1. –‰–Ϋ―²–Β–≥―Ä–Α–Μ―¨–Ϋ–Α―è –Φ–Ψ–¥–Β–Μ―¨ –Ω–Α―²–Ψ–≥–Β–Ϋ–Β–Ζ–Α –£–€–î
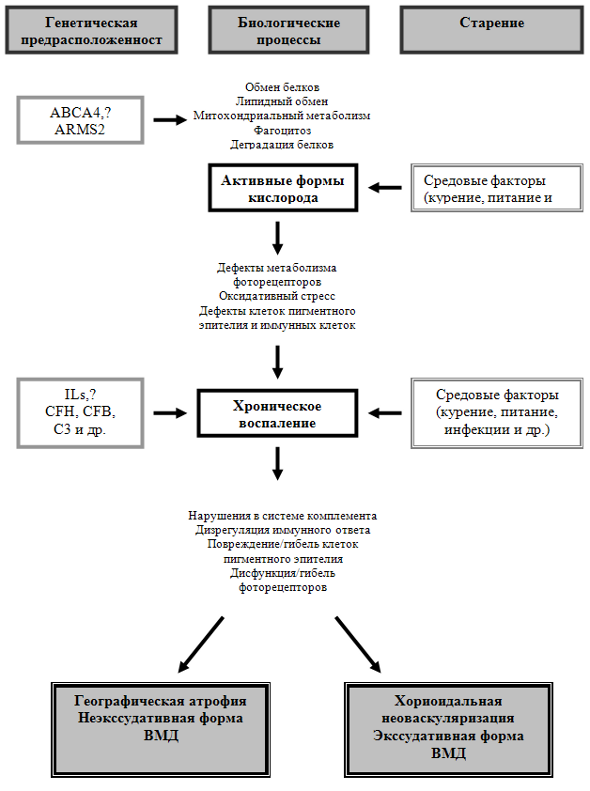
–Γ―²–Α―Ä–Β–Ϋ–Η–Β βÄ™ –Ω–Β―Ä–≤–Η―΅–Ϋ―΄–Ι ―³–Α–Κ―²–Ψ―Ä, –Ω―Ä–Η–≤–Ψ–¥―è―â–Η–Ι –Κ –Ω–Ψ–≤―Ä–Β–Ε–¥–Β–Ϋ–Η―è–Φ ―³–Ψ―²–Ψ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤ –Η –Κ–Μ–Β―²–Ψ–Κ ―Ä–Β―²–Η–Ϋ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ω–Η–≥–Φ–Β–Ϋ―²–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è; ―ç―²–Η –Ω–Ψ–≤―Ä–Β–Ε–¥–Β–Ϋ–Η―è ―¹–≤―è–Ζ–Α–Ϋ―΄ ―¹ ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Φ–Η –≥–Β–Ϋ–Β―²–Η―΅–Β―¹–Κ–Η–Φ–Η –Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η―è–Φ–Η. –ö–Ψ–Φ–Ω–Μ–Β–Φ–Β–Ϋ―² –Η –Η–Φ–Φ―É–Ϋ–Ϋ―΄–Ι –Ψ―²–≤–Β―² ―²–Α–Κ–Ε–Β –Η–≥―Ä–Α―é―² –≤–Α–Ε–Ϋ―É―é ―Ä–Ψ–Μ―¨ –≤ –≤–Ψ–Ζ–Ϋ–Η–Κ–Ϋ–Ψ–≤–Β–Ϋ–Η–Η –Η –Ω―Ä–Ψ–≥―Ä–Β―¹―¹–Η―Ä–Ψ–≤–Α–Ϋ–Η–Η –£–€–î [1].
–†–Η―¹. 2. –Γ―Ö–Β–Φ–Α―²–Η―΅–Β―¹–Κ–Ψ–Β –Η–Ζ–Ψ–±―Ä–Α–Ε–Β–Ϋ–Η–Β ―Ö―Ä–Ψ–Φ–Ψ―¹–Ψ–Φ ―΅–Β–Μ–Ψ–≤–Β–Κ–Α
–ü–Ψ–Κ–Α–Ζ–Α–Ϋ―΄ –Μ–Ψ–Κ―É―¹―΄, –Φ―É―²–Α―Ü–Η–Η –Κ–Ψ―²–Ψ―Ä―΄―Ö –Ω―Ä–Η–≤–Ψ–¥―è―² –Κ ―Ä–Α–Ζ–≤–Η―²–Η―é –£–€–î.
–†–Η―¹. 3. –Γ―Ö–Β–Φ–Α―²–Η―΅–Β―¹–Κ–Ψ–Β –Η–Ζ–Ψ–±―Ä–Α–Ε–Β–Ϋ–Η–Β –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ü–Η–Κ–Μ–Α
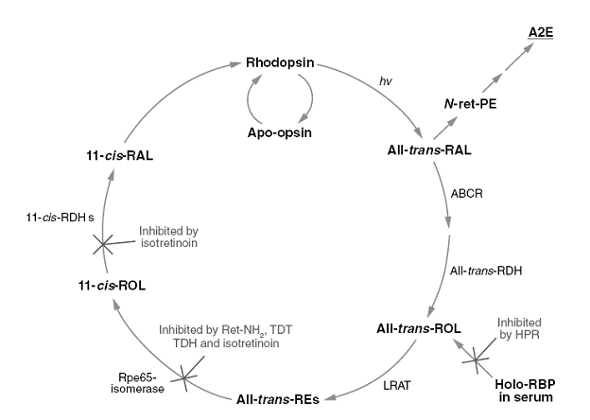
–‰–Μ–Μ―é―¹―²―Ä–Η―Ä―É–Β―² ―²–Ψ―΅–Κ–Η –Ω―Ä–Η–Μ–Ψ–Ε–Β–Ϋ–Η―è –Η–Ϋ–≥–Η–±–Η―²–Ψ―Ä–Ψ–≤ –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η―è, N-―Ä–Β―²–Η–Ϋ–Η–Μ–Η–¥–Η–Ϋ-N-―Ä–Β―²–Η–Ϋ–Η–Μ ―ç―²–Α–Ϋ–Ψ–Μ–Α–Φ–Η–Ϋ–Α (–ê2–ï).
–ü–Ψ–Μ–Ϋ–Ψ―¹―²―¨―é-―²―Ä–Α–Ϋ―¹-―Ä–Β―²–Η–Ϋ–Α–Μ―¨, –≤―΄―¹–≤–Ψ–±–Ψ–Ε–¥–Α–Β–Φ―΄–Ι –Ω―Ä–Η ―³–Ψ―²–Ψ–Η–Ζ–Η–Φ–Β―Ä–Η–Ζ–Α―Ü–Η–Η ―Ä–Ψ–¥–Ψ–Ω―¹–Η–Ϋ–Α, ―¹–Ψ–Β–¥–Η–Ϋ―è–Β―²―¹―è ―¹ ―³–Ψ―¹―³–Α―²–Η–¥–Η–Μ―ç―²–Α–Ϋ–Ψ–Μ–Α–Φ–Η–Ϋ–Ψ–Φ (PE) –≤ –Φ–Β–Φ–±―Ä–Α–Ϋ–Α―Ö –¥–Η―¹–Κ–Ψ–≤, –Ψ–±―Ä–Α–Ζ―É―è –Ω―Ä–Η ―ç―²–Ψ–Φ N-―Ä–Β―²–Η–Μ–Η–¥–Η–Ϋ-PE (N-ret-PE). –½–Α―²–Β–Φ ―¹–Ψ–Β–¥–Η–Ϋ–Β–Ϋ–Η–Β N-ret-PE ―¹ –¥―Ä―É–≥–Η–Φ –Ω–Ψ–Μ–Ϋ–Ψ―¹―²―¨―é-―²―Ä–Α–Ϋ―¹-―Ä–Β―²–Η–Ϋ–Α–Μ–Β–Φ, ―¹–Μ–Β–¥―É―é―â–Β–Β –Ζ–Α ―ç–Μ–Β–Κ―²―Ä–Ψ―Ü–Η–Κ–Μ–Η–Ζ–Α―Ü–Η–Β–Ι, –≥–Η–¥―Ä–Ψ–Μ–Η–Ζ–Ψ–Φ ―³–Ψ―¹―³–Α―²–Ϋ―΄―Ö ―ç―³–Η―Ä–Ψ–≤ –Η –Ψ–Κ–Η―¹–Μ–Β–Ϋ–Η–Β–Φ, –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η―é –ê2–ï. –Λ–Α―Ä–Φ–Α–Κ–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–Β –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Ψ, –Κ–Ψ―²–Ψ―Ä–Ψ–Β ―É–Φ–Β–Ϋ―¨―à–Α–Β―² ―¹–≤–Β―²-–Η–Ϋ–¥―É―Ü–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–Β –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η–Β –Ω–Ψ–Μ–Ϋ–Ψ―¹―²―¨―é-―²―Ä–Α–Ϋ―¹-―Ä–Β―²–Η–Ϋ–Α–Μ―è, –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ–Φ―É ―¹–Ϋ–Η–Ε–Β–Ϋ–Η―é –≤–Β―Ä–Ψ―è―²–Ϋ–Ψ―¹―²–Η ―ç―²–Ψ–≥–Ψ –≤―²–Ψ―Ä–Ψ–≥–Ψ –Ω―Ä–Η―¹–Ψ–Β–¥–Η–Ϋ–Β–Ϋ–Η―è –Η –Ζ–Α–Φ–Β–¥–Μ―è–Β―² –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η–Β –ê2–ï. N-(4-–≥–Η–¥―Ä–Ψ–Κ―¹–Η―³–Β–Ϋ–Η–Μ)-―Ä–Β―²–Η–Ϋ–Α–Φ–Η–¥ (HPR) –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ ―¹–Ϋ–Η–Ε–Β–Ϋ–Η―é ―É―Ä–Ψ–≤–Ϋ―è ―Ä–Β―²–Η–Ϋ–Ψ–Μ―¹–≤―è–Ζ―΄–≤–Α―é―â–Β–≥–Ψ –±–Β–Μ–Κ–Α (RBP) –≤ –Ω–Μ–Α–Ζ–Φ–Β. Rpe65-–Ψ–Ω–Ψ―¹―Ä–Β–¥–Ψ–≤–Α–Ϋ–Ϋ–Α―è –Η–Ζ–Ψ–Φ–Β―Ä–Η–Ζ–Α―Ü–Η―è –Φ–Ψ–Ε–Β―² –±―΄―²―¨ –±–Μ–Ψ–Κ–Η―Ä–Ψ–≤–Α–Ϋ–Α ―¹ –Ω–Ψ–Φ–Ψ―â―¨―é ―Ä–Β―²–Η–Ϋ–Η–Μ–Α–Φ–Η–Ϋ–Α (Ret-NH2), ―³–Α―Ä–Ϋ–Β―¹–Η–Μ―¹–Ψ–¥–Β―Ä–Ε–Α―â–Η―Ö –Α–Ϋ–Α–Μ–Ψ–≥–Ψ–≤, TDH –Η TDT, –Η–Ζ–Ψ―²―Ä–Β―²–Η–Ϋ–Ψ–Η–Ϋ–Α. –‰–Ζ–Ψ―²―Ä–Β―²–Η–Ϋ–Ψ–Η–Ϋ ―²–Α–Κ–Ε–Β –Η–Ϋ–≥–Η–±–Η―Ä―É–Β―² 11-―Ü–Η―¹-―Ä–Β―²–Η–Ϋ–Ψ–Μ –¥–Β–≥–Η–¥―Ä–Ψ–≥–Β–Ϋ–Α–Ζ―É (11-cis-RDH)
–†–Η―¹. 4. –€–Ψ–¥―É–Μ–Η―Ä―É―é―â–Η–Β –¥–Β–Ι―¹―²–≤–Η–Β ―³–Η–±―É–Μ–Η–Ϋ–Ψ–≤
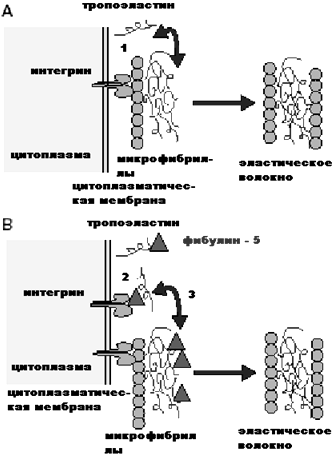
–£–Ζ–Α–Η–Φ–Ψ–¥–Β–Ι―¹―²–≤–Η–Β ―³–Η–±―É–Μ–Η–Ϋ–Α 5 (–Η–Ζ–Ψ–±―Ä–Α–Ε―ë–Ϋ –≤ ―³–Ψ―Ä–Φ–Β ―²―Ä–Β―É–≥–Ψ–Μ―¨–Ϋ–Η–Κ–Α) ―¹ –¥–Η–Ϋ–Α–Φ–Η―΅–Β―¹–Κ–Η–Φ–Η –Η–Ϋ―²–Β–≥―Ä–Η–Ϋ–Ψ–≤―΄–Φ–Η ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Α–Φ–Η, –Α ―²–Α–Κ–Ε–Β ―¹ ―²―Ä–Ψ–Ω–Ψ―ç–Μ–Α―¹―²–Η–Ϋ–Ψ–Φ; –≤–Μ–Η―è–Ϋ–Η–Β ―³–Η–±―É–Μ–Η–Ϋ–Α 5 –Ϋ–Α ―³–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β ―ç–Μ–Α―¹―²–Η―΅–Β―¹–Κ–Η―Ö –≤–Ψ–Μ–Ψ–Κ–Ψ–Ϋ –Η ―¹–Ψ–±–Η―Ä–Α–Ϋ–Η–Β –Φ–Η–Κ―Ä–Ψ―³–Η–±―Ä–Η–Μ–Μ –≤ –Ψ–Ω―Ä–Β–¥–Β–Μ―ë–Ϋ–Ϋ―΄–Β ―¹―²―Ä―É–Κ―²―É―Ä―΄, –Α –Η–Φ–Β–Ϋ–Ϋ–Ψ: ―³–Η–±―É–Μ–Η–Ϋ―΄ ―É―΅–Α―¹―²–≤―É―é―² –≤ ―³–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Ϋ–Η–Η –Κ–Μ–Β―²–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ψ―²–≤–Β―²–Α –≤ –≤–Η–¥–Β –Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η―è ―Ä–Ψ―¹―²–Α, –Φ–Ψ―Ä―³–Ψ–Μ–Ψ–≥–Η–Η –Η ―¹―²―Ä–Ψ–Β–Ϋ–Η―è –Κ–Μ–Β―²–Ψ―΅–Ϋ―΄―Ö ―¹―²―Ä―É–Κ―²―É―Ä. –ü―Ä–Η ―ç―²–Ψ–Φ ―³–Η–±―É–Μ–Η–Ϋ―΄ –Ζ–Α–¥–Β–Ι―¹―²–≤–Ψ–≤–Α–Ϋ―΄ –Ϋ–Β ―²–Ψ–Μ―¨–Κ–Ψ –≤ –≤–Ψ―¹–Ω―Ä–Η―è―²–Η–Η –Η –Ω–Β―Ä–Β–¥–Α―΅–Β ―¹–Η–≥–Ϋ–Α–Μ–Ψ–≤ –Ψ―² –Η–Ϋ―²–Β–≥―Ä–Η–Ϋ–Ψ–≤ –Κ –Φ–Β–Ε–Κ–Μ–Β―²–Ψ―΅–Ϋ–Ψ–Φ―É –Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ―¹―²–≤―É –Φ–Β–Φ–±―Ä–Α–Ϋ―΄ –ë―Ä―É―Ö–Α, –Ϋ–Ψ –Η –≤ –Ψ–±―Ä–Α―²–Ϋ–Ψ–Ι –Ω–Β―Ä–Β–¥–Α―΅–Β ―ç―²–Η―Ö ―¹–Η–≥–Ϋ–Α–Μ–Ψ–≤ –Κ –≤–Ϋ―É―²―Ä–Η–Κ–Μ–Β―²–Ψ―΅–Ϋ―΄–Φ –Κ–Ψ–Φ–Ω–Ψ–Ϋ–Β–Ϋ―²–Α–Φ.
–†–Η―¹. 5. –½–Ϋ–Α―΅–Β–Ϋ–Η–Β PPAR ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤ –≤ –Ω―Ä–Β–¥―É–Ω―Ä–Β–Ε–¥–Β–Ϋ–Η–Η ―Ä–Α–Ζ–≤–Η―²–Η―è –£–€–î
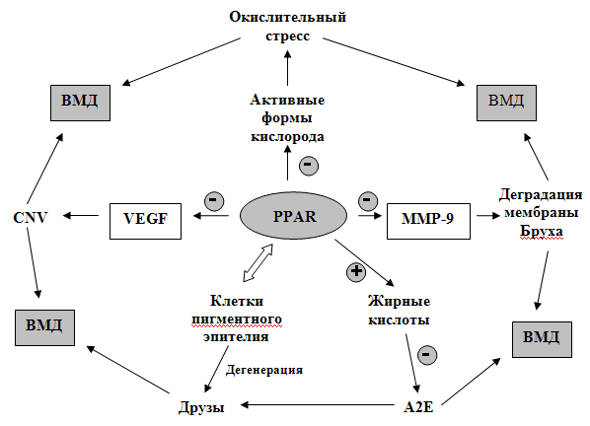
–¦–Η–≥–Α–Ϋ–¥–Α–Φ–Η PPAR ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤ ―è–≤–Μ―è―é―²―¹―è –Ε–Η―Ä–Ϋ―΄–Β –Κ–Η―¹–Μ–Ψ―²―΄. –Θ –Ζ–¥–Ψ―Ä–Ψ–≤–Ψ–≥–Ψ ―΅–Β–Μ–Ψ–≤–Β–Κ–Α PPAR ―¹–≤―è–Ζ―΄–≤–Α―é―² –Η―Ö, –Ϋ–Ψ ―¹ –≤–Ψ–Ζ―Ä–Α―¹―²–Ψ–Φ –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤ ―¹–Ϋ–Η–Ε–Α–Β―²―¹―è, –Ω―Ä–Ψ–Η―¹―Ö–Ψ–¥–Η―² –Ϋ–Α–Κ–Ψ–Ω–Μ–Β–Ϋ–Η–Β –Ε–Η―Ä–Α, –Μ–Η–Ω–Ψ―³―É―¹―Ü–Η–Ϋ–Α (–≥–Μ–Α–≤–Ϋ―΄–Ι –Κ–Ψ–Φ–Ω–Ψ–Ϋ–Β–Ϋ―² –±–Η―¹―Ä–Β―²–Η–Ϋ–Ψ–Η–¥ –ê2–ï), ―΅―²–Ψ –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η―é –¥―Ä―É–Ζ –Η ―Ä–Α–Ζ–≤–Η―²–Η―é –£–€–î. –ê–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ PPAR ―É–Φ–Β–Ϋ―¨―à–Α–Β―² ―ç–Κ―¹–Ω―Ä–Β―¹―¹–Η―é –Φ–Α―²―Ä–Η–Κ―¹–Ϋ–Ψ–Ι –Φ–Β―²–Α–Μ–Μ–Ψ–Ω―Ä–Ψ―²–Β–Η–Ϋ–Α–Ζ―΄ (–€–€–†-9), –Κ–Ψ―²–Ψ―Ä–Α―è –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ –¥–Β–≥―Ä–Α–¥–Α―Ü–Η–Η –Φ–Β–Φ–±―Ä–Α–Ϋ―΄ –ë―Ä―É―Ö–Α, –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η―é ―¹–Ψ―¹―É–¥–Ψ–≤ ―¹ ―Ö―Ä―É–Ω–Κ–Η–Φ–Η ―¹―²–Β–Ϋ–Κ–Α–Φ–Η. –€–€–† βÄ™ –Ω―Ä–Ψ―²–Β–Α–Ζ–Α, ―¹–Η–Ϋ―²–Β–Ζ–Η―Ä―É–Β–Φ–Α―è –Κ–Μ–Β―²–Κ–Α–Φ–Η-–Φ–Α–Κ―Ä–Ψ―³–Α–≥–Α–Φ–Η, ―Ä–Α–Ζ―Ä―É―à–Α–Β―² –≤–Ϋ–Β–Κ–Μ–Β―²–Ψ―΅–Ϋ―΄–Ι –Φ–Α―²―Ä–Η–Κ―¹. –Δ–Α–Κ–Ε–Β PPAR ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä―΄ –Η–Ϋ–≥–Η–±–Η―Ä―É―é―² (–Ω―É―²―ë–Φ –Α–Κ―²–Η–≤–Α―Ü–Η–Η ―²―Ä–Α–Ϋ―¹–Κ―Ä–Η–Ω―Ü–Η–Η –Α–Ϋ―²–Η–Ψ–Κ―¹–Η–¥–Α–Ϋ―²–Ϋ―΄―Ö –≥–Β–Ϋ–Ψ–≤, ―²–Α–Κ–Η―Ö –Κ–Α–Κ –≥–Μ―É―²–Α–Φ–Α―²-―Ü–Η―¹―²–Β–Η–Ϋ –Μ–Η–≥–Α–Ζ―΄) –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η–Β ―¹–≤–Ψ–±–Ψ–¥–Ϋ―΄―Ö ―³–Ψ―Ä–Φ –Κ–Η―¹–Μ–Ψ―Ä–Ψ–¥–Α (–Ω–Β―Ä–Ψ–Κ―¹–Η–¥–Α –≤–Ψ–¥–Ψ―Ä–Ψ–¥–Α, ―¹–≤–Ψ–±–Ψ–¥–Ϋ–Ψ–≥–Ψ –Κ–Η―¹–Μ–Ψ―Ä–Ψ–¥–Α, ―²–Ψ–Κ―¹–Η―΅–Ϋ―΄―Ö ―Ä–Α–¥–Η–Κ–Α–Μ–Ψ–≤ –Κ–Η―¹–Μ–Ψ―Ä–Ψ–¥–Α), –Κ–Ψ―²–Ψ―Ä―΄–Β –Ω―Ä–Η–≤–Ψ–¥―è―² –Κ –Ψ–Κ–Η―¹–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–Φ―É ―¹―²―Ä–Β―¹―¹―É –Η ―Ä–Α–Ζ–≤–Η―²–Η―é –£–€–î. PPAR ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä―΄ –Η–Ϋ–≥–Η–±–Η―Ä―É―é―² –Ω―Ä–Ψ–Μ–Η―³–Β―Ä–Α―Ü–Η―é ―ç–Ϋ–¥–Ψ―²–Β–Μ–Η–Α–Μ―¨–Ϋ―΄―Ö –Κ–Μ–Β―²–Ψ–Κ, –≤―΄–Ζ–≤–Α–Ϋ–Ϋ―É―é –¥–Β–Ι―¹―²–≤–Η–Β–Φ ―³–Α–Κ―²–Ψ―Ä–Α ―Ä–Ψ―¹―²–Α ―ç–Ϋ–¥–Ψ―²–Β–Μ–Η―è ―¹–Ψ―¹―É–¥–Ψ–≤ (VEGF). –Δ–Α–Κ–Η–Φ –Ψ–±―Ä–Α–Ζ–Ψ–Φ, ―²–Ψ―Ä–Φ–Ψ–Ζ–Η―²―¹―è –Ω―Ä–Ψ―Ü–Β―¹―¹ –Ϋ–Β–Ψ–≤–Α―¹–Κ―É–Μ―è―Ä–Η–Ζ–Α―Ü–Η–Η (CNV) –Η ―Ä–Α–Ζ–≤–Η―²–Η–Β ―ç–Κ―¹―¹―É–¥–Α―²–Η–≤–Ϋ–Ψ–Ι ―³–Ψ―Ä–Φ―΄ –£–€–î.
–¦–Η―²–Β―Ä–Α―²―É―Ä–Α
1. Anand Swaroop, Emily Y. Chew, Catherine Bowes Rickman, and Goncalo R. Abecasis. Unraveling a Multifactorial Late-Onset Disease: From Genetic Susceptibility to Disease Mechanisms for Age-Related Macular Degeneration. Annu Rev Genomic Hum Genet 2009; 10:19-43.
2. Klaver C. C., Wolts R. S., Vingerling J. R. et al. Arch Ophthalmol 1998; 116:653βÄ™8.
3. Klein R., Klein B. E. K., Lee K. E., et al. Changes in visual acuity in population over a 10βÄ™ year period. The Beaver Dam Study. Ophthalmol 2001; 108: 1757βÄ™66.
4. Williams R. A., Brady B. L., Thomas R. J. The psychosocial impact of macular degeneration. Arch Ophthalmol 1998; 116 (4):514βÄ™20.
5. Hyman L., Schachat A.P., He Q., Leske M.CArch Ophthalmol 2000; 188(4):351βÄ™8.
6. Edwin M. Stone, M.D., Ph.D., Terry A. Braun, Ph.D., Stephen R. Russell, M.D.,
Markus H. Kuehn, Ph.D., Andrew J. Lotery, M.D., Paula A. Moore. Missense Variations in the Fibulin 5 Gene and Age-Related Macular Degeneration. NEJM 2004; 351 ( 4):346-53.
7. Stuart L. Fine, M. D., Jeffrey W. Berger, M. D., Ph. D., Maureen G. Maguire, Ph. D., and Allen C. Ho, M. D. Age-Related Macular Degeneration. 2000; 342 (7); 483-91.
8. Edwin M. Stone. Macular Degeneration. Annu Rev Med βÄ™ 2007; 58:477βÄ™90.
9. –¦.–ê. –ö–Α―Ü–Ϋ–Β–Μ―¨―¹–Ψ–Ϋ –ö–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Η–Ι –Α―²–Μ–Α―¹ –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Η –≥–Μ–Α–Ζ–Ϋ–Ψ–≥–Ψ –¥–Ϋ–Α. 2008 –≥, ―¹―²―Ä. 59
10. –Γ.–≠.–ê–≤–Β―²–Η―¹–Ψ–≤, –ï.–ê.–ï–≥–Ψ―Ä–Ψ–≤, –û―³―²–Α–Μ―¨–Φ–Ψ–Μ–Ψ–≥–Η―è: –Ϋ–Α―Ü–Η–Ψ–Ϋ–Α–Μ―¨–Ϋ–Ψ–Β ―Ä―É–Κ–Ψ–≤–Ψ–¥―¹―²–≤–Ψ, 2008 –≥, ―¹―²―Ä.623-637.
11. Jeganathan VS, Verma N. Safety and efficacy of intravitreal anti-VEGF injections for age-related macular degeneration. Curr Opin Ophthalmol. 2009; 20:223-5.
12. Bylsma Guy W., Guymer Robyn H. –ê–≤―¹―²―Ä–Α–Μ–Η―è Clin Exp Optom 2005; 88: 5: 322βÄ™334
13. Brown DM, Michels M, Kaiser PK, Heier JS, Sy JP, Ianchulev T. Ranibizumab versus verteporfin photodynamic therapy for age-related macular degeneration: Two-year results of the ANCHOR study. Ophthalmology. 2009; 116:57-65.
14. –î–Α–Μ―¨ –ù. –°. –€–Α–Κ―É–Μ―è―Ä–Ϋ―΄–Β –Κ–Α―Ä–Ψ―²–Η–Ϋ–Ψ–Η–¥―΄. –€–Ψ–≥―É―² –Μ–Η –Ψ–Ϋ–Η –Ζ–Α―â–Η―²–Η―²―¨ –Ϋ–Α―¹ –Ψ―² –≤–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Ψ–Ι –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η–Η? –û―³―²–Α–Μ―¨–Φ –≤–Β–¥–Ψ–Φ–Ψ―¹―²–Η 2008; 1 (3): 51βÄ™3.
15. –¦.–£. –•―É―Ä–Α–≤–Μ―ë–≤–Α, –Γ.–ê. –ö–Ψ―¹–Κ–Η–Ϋ, –ï.–°. –ë―É–Ζ–Η–Ϋ–Α, –ê.–£.–·–Ϋ, –ê.–£. –‰–≤–Α–Ϋ–Ψ–≤–Α, –Γ.–€. –ê–≤–Β―²–Η―¹―è–Ϋ, –€–Ψ–Ϋ–Η―²–Ψ―Ä–Η–Ϋ–≥ –±–Ψ–Μ―¨–Ϋ―΄―Ö –≤–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Ψ–Ι –Φ–Α–Κ―É–Μ–Ψ–¥–Η―¹―²―Ä–Ψ―³–Η–Β–Ι –Ω―Ä–Η –Κ–Ψ–Φ–Ω–Μ–Β–Κ―¹–Ϋ–Ψ–Φ –Η―Ö –Μ–Β―΅–Β–Ϋ–Η–Η –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α–Φ–Η ―Ä–Α―¹―²–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –Ω―Ä–Ψ–Η―¹―Ö–Ψ–Ε–¥–Β–Ϋ–Η―è. –†–Ψ―¹―¹–Η–Ι―¹–Κ–Η–Ι –Φ–Β–¥–Η―Ü–Η–Ϋ―¹–Κ–Η–Ι –Ε―É―Ä–Ϋ–Α–Μ, –ö–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Α―è –Ψ―³―²–Α–Μ―¨–Φ–Ψ–Μ–Ψ–≥–Η―è 2008; 9 (1):24-6.
16. –Γ.–≠.–ê–≤–Β―²–Η―¹–Ψ–≤, –Δ.–ù. –ö–Η―¹–Β–Μ―ë–≤–Α, –°.–€.–¦–Α–≥―É―²–Η–Ϋ–Α, –ï.–ê.–ö―Ä–Α–≤―΅―É–Κ, –£–Μ–Η―è–Ϋ–Η–Β –≤–Α–Ζ–Ψ–Α–Κ―²–Η–≤–Ϋ―΄―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ –Ϋ–Α –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ―΄–Β ―³―É–Ϋ–Κ―Ü–Η–Η –Η –≥–Μ–Α–Ζ–Ϋ–Ψ–Ι –Κ―Ä–Ψ–≤–Ψ―²–Ψ–Κ ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö ―¹ ―Ä–Α–Ϋ–Ϋ–Η–Φ–Η –Ω―Ä–Ψ―è–≤–Μ–Β–Ϋ–Η―è–Φ–Η –≤–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Ψ–Ι –Φ–Α–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –¥–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η–Β–Ι. –£–Β―¹―²–Ϋ–Η–Κ –Ψ―³―²–Α–Μ―¨–Φ–Ψ–Μ–Ψ–≥–Η–Η 2007; 3:
17. –Δ.–ù. –€–Α–Μ–Η―à–Β–≤―¹–Κ–Α―è, –‰.–™. –î–Ψ–Μ–≥–Ψ–≤–Α, –≠.–ê.–û―Ä―²–Β–Ϋ–±–Β―Ä–≥, –‰–Ζ―É―΅–Β–Ϋ–Η–Β –≤–Μ–Η―è–Ϋ–Η―è –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ –Γ―²―Ä–Η–Κ―¹ –Η –Γ―²―Ä–Η–Κ―¹ ―³–Ψ―Ä―²–Β –Ϋ–Α –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ―΄–Β ―³―É–Ϋ–Κ―Ü–Η–Η –±–Ψ–Μ―¨–Ϋ―΄―Ö ―¹ –≤–Ψ–Ζ―Ä–Α―¹―²–Ϋ–Ψ–Ι –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Β–Ι ―¹–Β―²―΅–Α―²–Κ–Η –Η –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –Ϋ–Β―Ä–≤–Α. –†–Ψ―¹―¹–Η–Ι―¹–Κ–Η–Ι –Φ–Β–¥–Η―Ü–Η–Ϋ―¹–Κ–Η–Ι –Ε―É―Ä–Ϋ–Α–Μ, –ö–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Α―è –Ψ―³―²–Α–Μ―¨–Φ–Ψ–Μ–Ψ–≥–Η―è 2008; 9 (1): 20-4.
18. Janis Lem. Diseases of G-Protein-Coupled Signal Transduction Pathways: The Mammalian Visual System as a Model. 1998; Seminars in Neuroscience 9, Article No. SN980126; 232-8.
19. Olaf Strauss. The Petinal Pigmentum Epithelium in Visual Function. 2005, Physiol Rev 85:845-881; pp. 845-865.
20. Gabriel H. Travis, Marcin Golczak, Alexander R. Moise, and Krzysztof Palczewski. Diseases Caused by Defects in the Visual Cycle: Retinoids as Potential Therapeutic Agents. Annu Rev Pharmacol Toxicol 2007; 47:469-512.
21. Nathan L. Mata, Walid N. Moghrabi, Jung S. Lee et. al. Rpe65 Is a Retinyl Ester Binding Protein That Presents Insoluble Substrate to the Isomerase in Retinal Pigment Epithelial Cells. 2004; 279 (1) Issue of January 2: 635-42.
22. Janet R. Sparrow. Therapy for macular degeneration: Insights from acne. 2003; 100: 8: 4353-4.
23. Kim S. Midwood and Jean E. Schwarzbauer Elastic Fibers: Building Bridges Between Cells and Their Matrix. Current Biology 2002; 12: R279βÄ™R281.
24. Erythropoetin βÄ™ An Endogenous Retinal Survival Factor. N Engl J Med 2002; 347 (24): 1968-70.
25. Marisol del V Cano and Peter L.Gehlbach. PPAR Ligands as Potential Therapeutic Agents for Wet Age-Related Macular Degeneration. Hindawi Publishing Corporation, PPAR Reseach, Vol. 2008, article ID 821592.
26. AlexandraA.Herzlich, JingshengTuo andChi-ChaoChan. Peroxisome Prolife rator-Activated Receptor and Age-RelatedMacularDegeneration. Hindawi Publishing Corporation, PPAR Reseach, Vol. 2008, article ID 389507.