Последние достижения в области медицинских биотехнологий стимулируют мировое медицинское сообщество и фармакологические компании к переходу на новый уровень терапевтической практики. Если ранее целью создания лекарственного средства служил химический синтез молекул, эффективных для лечения больших популяций больных, то на современном этапе внимание сконцентрировано на создании препаратов методами биотехнологий, прицельно воздействующих на патогенетические механизмы развития болезни. Другими словами, мы – на пороге создания и развития таргетной, персонифицированной терапии, когда необходимый препарат в нужной дозе и в нужное время воздействует на конкретного пациента [1].
Биофармацевтические лекарственные средства представлены «семействами»:
- гормонов и ферментов (инсулин, соматотропный гормон, фолликулостимулирующий гормон и т.д.),
- цитокинов (препараты интерферонов) и белков (низкомолекулярные гепарины),
- вакцин,
- моноклональных антител (моноклональные антитела к ФНО-альфа, к Jg класса Е),
- антисмысловых лекарственных средств,
- препаратов клеточной терапии.
Как, по истечении срока патента на оригинальное лекарственное средство появляется возможность регистрации дженериков, так же, и в случае биологических агентов – открываются возможности для применения биоаналогов[2,3]. Однако биоаналоги (от англ. biosimilars) и дженерики не являются синонимами в плане идентичности – молекулярного соответствия оригинальному препарату, и имеют существенные отличия, представленные в таблице[4].
Таблица. Основные различия между дженериком и биоаналогом
| Дженерик | Биоаналог |
|---|---|
| небольшая молекулярная масса с чётко установленной химической формулой | белки с высокой молекулярной массой |
| производство путём химического синтеза | производство с использованием методов генной инженерии в культуре живых клеток |
| высокая стабильность молекулы | менее стабильны |
| проведение упрощённой процедуры клинических исследований | необходимость проведения полного цикла доклинических и клинических исследований |
| замена на оригинальный препарат происходит без ущерба для терапии | замена невозможна |
Безусловно, создание биоаналогов инновационных биофармацевтических продуктов, является весьма перспективным в глобальной медицинской фармацевтической индустрии. Предполагаемый успех на рынке лекарственных средств связан прежде всего с «патентным обвалом» оригинальных препаратов в ближайшие 5 лет, с ростом ежегодного применения биопрепаратов на 12-15% и с более низкой стоимостью биоаналогов по сравнению с инновационными «агентами»(на 20-25% ниже), которые являются самыми дорогостоящими лекарственными средствами (рис. 1 и рис. 2).
Рисунок 1. Эволюция объема международных продаж на фармакологическом рынке 10 биопрепаратов-блокбастеров с 2004 по 2011 гг. (адаптировано Bruno Calo-Fernandez[2])
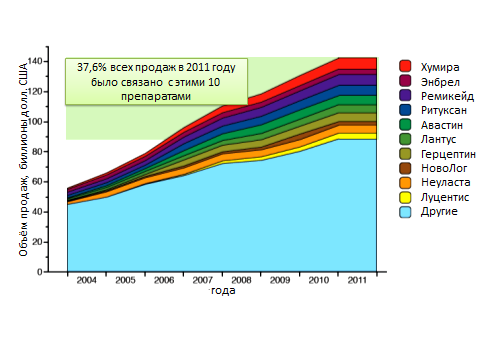
Рисунок 2. Мировая фармотрасль на примере 10 наиболее популярных брендов биопрепаратов (адаптировано по Bruno Calo-Fernandez[2]) С 2012 по 2019 гг. – окончание срока действия патентов для большинства биопрепаратов, обозначено желтым цветом. *Для препарата Enbrel (зарегистрирован в 1995г.) в 2011г. был продлён срок действия патента путем расширения показаний к применению.
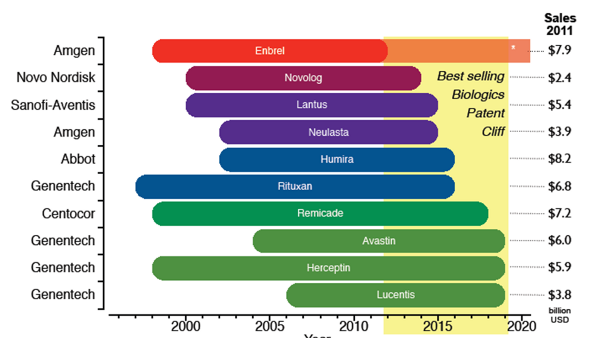
Таким образом, в звеньях фармкомпания-лечащий врач-пациент каждый заинтересован в создании и успешной регистации и применении биоаналогов. Однако на этом пути встречается множество проблем, связанных с
- биоэквивалентностью, терапевтической эквивалентностью и вопросами безопасности,
- регистрацией,
- ценообразованием[5].
Клонирование генетического материала человека и создание in vitro систем биологической продукции позволяет получать рекомбинантную ДНК для синтеза новых лекарственных средств – эквивалентов оригинальным хорошо известным препаратам. Однако воссоздание идентичного оригиналу препарата невозможно вследствие сложности процесса производства, включающего около 4 тысяч последовательных этапов, результатом которых может быть получение белка, отличающегося по структуре и иммуногенности. Так, в США при применении биоаналога гепарина, разработанного Baxter, было зарегистрировано около 150 смертельных случаев вследствие непредвиденных иммунологических реакций[6]. В связи с этим невозможна экстраполяция данных клинических исследований, проведенных в отношении оригинала, на биоаналог. Это затрудняет и увеличивает длительность процесса регистации новых препаратов.
Представить общую картину места различных фармакологических компаний в стратегии развития рынка биофармацевтических препаратов можно следующим образом[5]:
- компании, разрабатывающие инновационные биопрепараты или следующие генерации биопрепаратов (т.н. «biobetters») – единственным лидером является Roche;
- компании, разрабатывающие биоаналоги оригинальных лекарственных препаратов – Novartis, Merck, Pfizer;
- компании-лидеры в производстве дженериков и в настоящее время проявляющие интерес к созданию биоаналогов – Teva, Hospira;
- новые «лица» на международном фармацевтическом рынке – Celltrion, Samsung.
Таким образом, несмотря на экономические преимущества, вопросы эффективности и безопасности неодназначны и требуют тщетельного изучения в каждом конкретном случае. Исходя из этого, законодательство, действующее во многих странах в отношении регистрации дженериков, неприменимо для биоаналогов и требует создания новой базы.
Так, мировые организации, осуществляющие контроль за лекарственными средствами (FDA, EMA) рассматривают и утверждают принципы одобрения аналогов биопрепаратов[7,8].
В России также назрела необходимость четкого нормативно-правового регулирования принципов трансляционной медицины. В настоящее время в Законе № 61 от 12.04.2010 «Об обращении лекарственных средств» нет даже упоминания о существовании «оригинальных биологических лекарственных средств» и «воспроизведенных биологических лекарственных средств». Вследствие вышеобозначенного, вопрос применения биоаналогов в российском здравоохранении требует незамедлительного решения. В отсутствии клинических исследований эффективности, безопасности и иммуногенности в дорегистрационном периоде биоаналоги представляют собой препараты с неизвестными свойствами и клиницисты не могут применять их.
Литература:
- Braido F, et al., From «blockbusters» to «biosimilars»: An opportunity for patients, medical specialists and health care providers, Pulmonary Pharmacology & Therapeutics (2012), http://dx.doi.org/10.1016/j.pupt.2012.09.005
- Bruno Calo-Fern`andez. Biosimilars: Company Strategies to Capture Value from the Biologics Market. Pharmaceuticals 2012, 5, 1393-1408; doi:10.3390/ph5121393.
- Хасабов Н.Н., Земскова Н.А. Биологические лекарственные средства и их биоаналоги: определение, вопросы качества, идентичности и безопасности. Вестн Росздравнадзора 2008; 6: 12—18.
- Christian K Schneider. Biosimilars in rheumatology: the wind of change. Ann Rheum Dis March 2013 Vol 72 No 3
- Deepa Dahal, MBA; John Doyle, Dr.P.H., MPH. An Integrated Approach to Biosimilar Development & Commercialization. http://www.quintiles.com/
- Usdin, S. The heparin story. Int. J. Risk Safety Med. 2009, 21, 93–103.
- Wang, J.; Chow, S. On the regulatory approval pathway of biosimilar products. Pharmaceuticals 2012, 5, 353–368.
- European Medicines Agency. Guideline on similar biological medicinal products containing monoclonal antibodies—non-clinical and clinical issues EMA/CHMP/BMWP/403543/2010.2012. http://www.ema.europa.eu/docs/en_GB/document_library/Scientific_guideline/2012/06/WC500128686.pdf (accessed 6 Jan 2013)