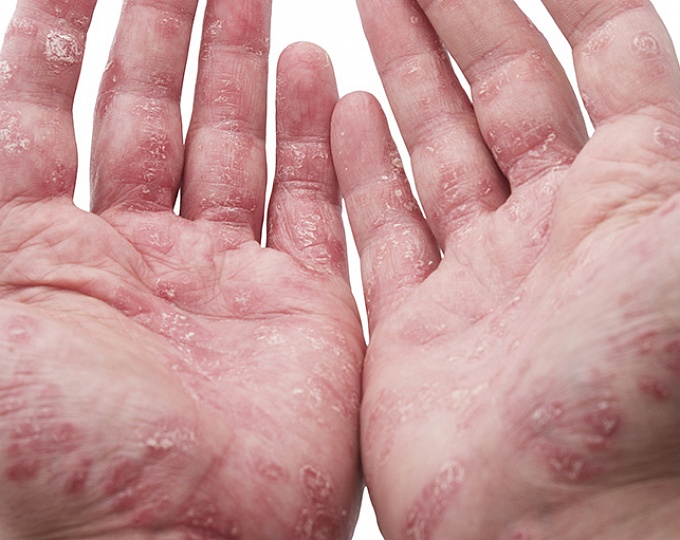
Актуальность
Псориаз - это хроническое иммуноопосредованное воспалительное заболевание кожи, встречающееся у 2% взрослых. Псориаз ассоциирован с ожирением, артериальной гипертензией, сахарным диабетом, гиперхолестеринемией и метаболическим синдромом.
Повоспалительней цитокин интерлейкин 23 играет ключевую роль в патогенезе псориаза через индукцию и поддержание Т хелперов 17 и 22, иннатных лимфоцитов, эффектора интерлейкина-17 и 22и ФНО-α.
Целью исследования было сравнить эффективность ризанкизумаба (BI 655066), гуманизированного IgG1 моноклонального антитела, которое подавляет интерлейкин 23 при воздействии на субъединицу p19, и устекинумаба, ингибитора интерлейкина 12 и 23 у пациентов с умеренно-тяжелым бляшковидным псориазом.
Методы
В исследование были рандомизированы 166 пациентов. Больные получали подкожно ризанкизумаб (однократно 18 мг на 0 неделе или 90 мг, или 180 мг на 0, 4 и 16 неделе) или устекинумаб (45 или 90 мг, согласно массе тела на 0, 4 и 16 неделе).
Первичной точкой в исследовании было выбрано 90% или большее снижение индекса Psoriasis Area and Severity Index (PASI) на 12 неделе.
Результаты
- На 12 неделе процент пациентов, имевших 90% или большее снижение суммы баллов по шкале PASI, составлю 77% (64 из 83 больных) в группе ризанкизумаба (90 мг и 180 мг объединено), по сравнению с 40% (у 16 из 40 пациентов) в группе устекинумаба (P<0.001). Процент больных, у которых отмечалось 100% снижение суммы баллов по шкале PASI был равен 45 и 18, соответственно.
- Эффективность терапии сохранялась в среднем на протяжении 20 недель после введения последней дозы ризанкизумаба в дозе 90 или 180 мг.
- В группе 18 мг или 90 мг ризанкизумаба и устекинумаба серьезные побочные эффекты наблюдались у 5 (12%), 6 (15%) и 3 пациентов (8%), соответственно. Нежелательные явления включила в себя 2 случая базальноклеточной карциномы и один случай серьезного сердечно-сосудистого события. В группе 180 мг ризанкизумаба серьезных побочных эффектов диагностировано не было.
Заключение
Во второй фазе клинического исследования было продемонстрировано, что селективное подавление интерлейкина 23 при помощи ризанкизумаба сопровождается более выраженным клиническим ответом, чем на фоне приема устекинумаба.
Продолжительность исследования и число пациентов не достаточны для того, чтобы сделать заключение о безопасности терапии.
Источник: Kim A. Papp, Andrew Blauvelt, Michael Bukhalo, et al. N Engl J Med 2017; 376:1551-1560.