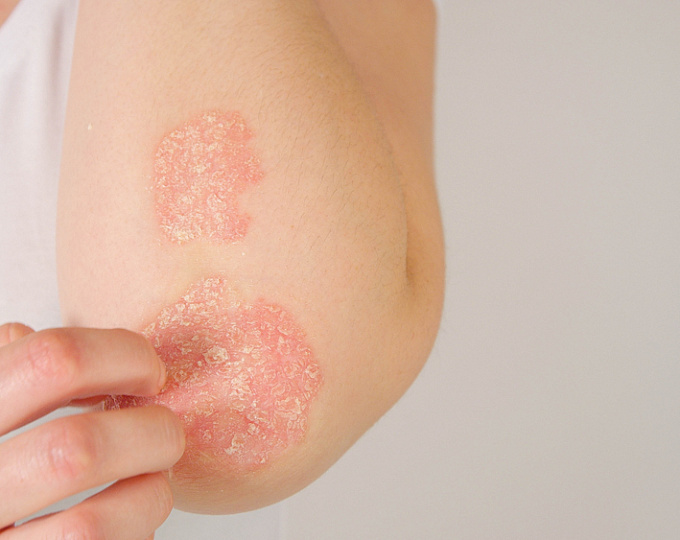
Актуальность
Препарат гуселькумаб, человеческое антитело, ингибитор интерлейкина-23, одобрен в июле 2020 года американским Food and Drug Administration для лечения взрослых пациентов с активным псориатическим артритом.
Отметим, что ранее в 2017 году препарат был одобрен для терапии бляшечного псориаза.
Одобрение препарата стало возможно после получения положительных результатов исследований DISCOVER-1 и DISCOVER-2.
Клинические исследования
- В исследования DISCOVER-1 и DISCOVER-2. были включены 1120 пациентов с активным псориатическим артритом, которые ранее не получали биологическую терапию или имели неполный ответ на 1 или 2 ингибитора фактора некроза опухоли альфа (примерно 30% пациентов).
- До включения в исследования пациенты получали апремиласт, болезнь-модифицирующий противоревматический препарат (почти 58% пациентов получали метотрексат) или НПВП.
Препарат использовали в дозе 100 мг подкожно каждые 8 недель, стартовая доза 100 мг на 0 и 4 неделе.
- Согласно результатам анализа, на фоне гуселькумаба достигалось 20% улучшение ответа по шкале American College of Rheumatology на 24 неделе. Частота ответа составила 52% в исследовании DISCOVER-1 и 64% в исследовании DISCOVER-2, в то время как в группе плацебо этот показатель составил 22% и 33%, соответственно.
- Показано, что терапия гуселькумабом улучшала такие показатели как кожные проявления псориаза, энтезит, дактилит и слабость.
Анализ безопасности
- Анализ безопасности препарата продемонстрировал, что у пациентов может повышаться риск развития бронхита и снижаться число нейтрофилов.
- В числе прочих нежелательных явлений отмечались инфекции верхних дыхательных путей, головная боль, реакция в месте инъекции, артралгия, диарея, гастроэнтерит, тинеа и инфекция herpes simplex.
Источник: Jeff Evans. FDA Approves Tremfya (Guselkumab) for Psoriatic Arthritis. Medscape. July 15, 2020.