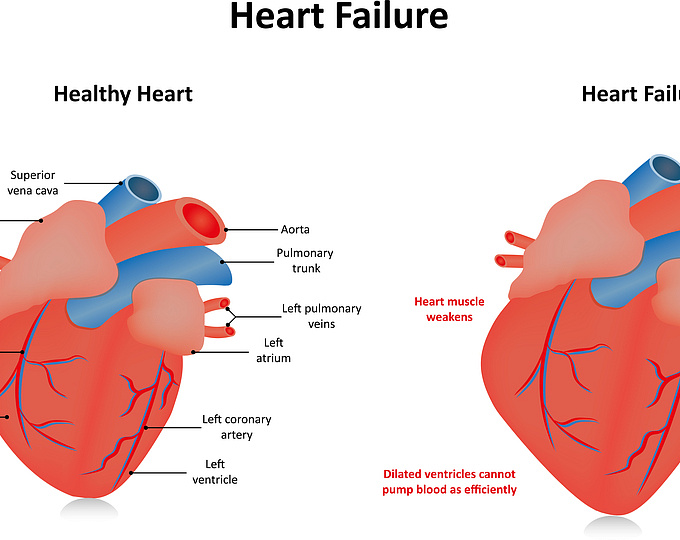
Актуальность
Несмотря на достигнутые успехи в лечении хронической сердечной недостаточности с низкой фракцией выброса, эффективная терапия хронической сердечной недостаточности с сохраненной фракцией выброса (ХСНсФВ) до сих пор отсутствует.
Милринон является ингибитором фосфодиэстеразы-3 и обладает вазодилатирующими свойствами. Недавно стала доступна пероральная форма препарата. В связи с чем целью исследования MilHFPEF стала оценка безопасности и эффективности милринона в отношении качества жизни и функционального статуса у пациентов с ХСНсФВ.
Методы
В рандомизированные двойное слепое плацебо контролируемое исследование включались пациенты с ХСНсФВ, установленной в соответствии с действующими Европейскими рекомендациями по ведению пациентов с сердечной недостаточностью. Кроме этого, обязательным критерием включения была госпитализация по поводу сердечной недостаточности в предыдущие 12 месяцев или повышение уровня BNP/NTproBNP>35/125 пг/мл, соответственно.
Пациенты рандомизировались в группы приема милринона и плацебо. Первичной конечной точкой эффективности было изменение в количестве баллов по Канзасскому опроснику, а первичной конечной точкой безопасности – развитие клинически значимых аритмий.
Результаты
-
В исследование было включено 23 пациента с ХСНсФВ.
-
Установлено, что количество баллов по Канзасскому опроснику значимо улучшилось в группе милринона в сравнении с плацебо (+10 против -3; p=0.046).
-
При этом значимых различий в изменении показателей теста 6-минутной ходьбы обнаружено не было.
-
Холтеровское мониторирование электрокардиограммы не выявило проаритмических эффектов милринона.
Заключение
Таким образом, результаты данного пилотного исследования при сопоставимом с плацебо профиле безопасности продемонстрировали возможную эффективность милринона у пациентов с ХСНсФВ. Вероятно, следующим шагом станет выполнение более крупного проспективного исследования, исходами в котором будут уже жесткие конечные точки.
Источник:
Nanayakkara S, et al. Journal of the American Heart Association. 2020. Doi: 10.1161/JAHA.119.015026