О проблеме вирусных гепатитов и прежде всего, вирусном гепатите В и вирусном гепатите С, как ни странно, несмотря на большое количество всевозможных конференций, существуют порой диаметрально противоположные представления. Во многом эти разночтения обусловлены тем, что мы не в полной мере владеем реальными данными статистики, отражающими заболеваемость вирусными гепатитами, и, в частности гепатитом В.
Итак, как часто мы выявляем лиц, инфицированных вирусом гепатита В (то есть частота выявления на 100 тысяч населения в год)? Если мы начнем свой отсчет с 2000 года, то носительство или число носителей на 100 тысяч населения в год составляло порядка 96 – очень высокая цифра. К 2007 году эта цифра опустилась вдвое – до 43. Острый гепатит в 1999 году диагностировался примерно у 43 человек на 100 тысяч населения в год, и эта частота существенно уменьшилась в 2007 году - в 8-9 раз (до 5 человек на 100 тысяч населения в год). Хронический гепатит В выявляется в пределах 5-7 человек на 100 тысяч населения в год (см. таблица 1).
Таблица 1. Заболеваемость вирусным гепатитом В в России.
| Выявление случаев | на 100 000/год |
| Носительства HBV-инфекции | |
| Острого гепатита В | 43,3 (1999) – 5,3 (2007) |
| Хронического гепатита В | 5,2 – 7,5 |
Когда мы с вами оперируем такими понятиями, как «носитель вируса гепатита В», «пациент с острым гепатитом В» и «пациент с хроническим гепатитом В», мы должны ясно представлять, что термин «носительство» или «носитель» – это очень лукавый термин. И в соответствии с многочисленными исследованиями как у нас в стране, так и за рубежом, подавляющее число так называемых носителей вируса гепатита В – это реальные пациенты, это реальные больные хроническим гепатитом В. Как сказала Анна Локк в своем выступлении на 13 Международном Симпозиуме по вирусным гепатитам и заболеваниям печени: «Сегодня вопрос стоит гораздо проще. Потенциально все инфицированные ВГВ являются кандидатами для противовирусной терапии, вопрос только в том, когда должно быть начато противовирусное лечение, чтобы оно было эффективным и рентабельным» [1]. Поэтому, если суммировать, скажем, носителей и выявляемых реальных пациентов с хроническим гепатитом В, то это, по всей вероятности, и будет отражать реальное число пациентов с хроническим гепатитом В. Что касается статистики, отражающей заболеваемость острым гепатитом В, то хорошо известно, что мы фиксируем преимущественно так называемые желтушные формы, которые составляют примерно треть от общего количества случаев острого вирусного гепатита. Но, так как в подавляющем большинстве случаев мы встречаемся с безжелтушной формой острого вирусного гепатита В, реальный учет заболеваемости острым вирусным гепатитом В чрезвычайно сложен.
Для успешной профилактики вирусного гепатита В необходимо знать, разумеется, пути инфицирования. Так, основными источниками инфекции инфекции являются больные острым гепатитом (примерно 4-6%), так называемые носители вируса гепатита В и больные хроническим гепатитом В (90-96%). Как мы подразделяем в структурном отношении этих носителей и пациентов, которые несут угрозу инфицирования других лиц? Вертикальный путь передач, то есть передача инфекции от матери ребенку колеблется в разных регионах от 1% до 35%, в зависимости от складывающихся условий в регионах. Переливание крови и компонентов крови стало минорным путем инфицирования благодаря принятым в последнее время мерам профилактики. Медицинские манипуляции продолжают оставаться довольно значительным путем инфицирования, и в этом отношении с медицинским персоналом, особенно с медицинскими сестрами, с хирургами необходимо проводить учебную работу, необходимо их вакцинировать. Каждый из практических врачей может вспомнить не один случай, когда медицинская сестра забирает кровь без перчаток. Довольно стандартная ситуация, к сожалению. И все-таки основным путем передачи инфекции сегодня являются половые контакты, так называемый промискуитет – беспорядочные половые контакты. Второй важнейший источник – это введение наркотических веществ, многократное использование шприца группой лиц, вводящих себе наркотики. Эти два пути передачи являются в настоящее время для нас доминирующими и составляют в целом от 33 до 87 %.
Надо отметить, что федеральная программа вакцинации, которая принята в нашей стране, сыграла свою положительную роль. Существует национальный календарь профилактических прививок. Всем новорожденным должны делаться прививки противовирусной вакциной: первую вакцинацию выполняют в первые 12 часов жизни, вторую - в возрасте одного месяца и третью – в возрасте 6 месяцев. Безусловно, к этой программе подключаются все желающие – вакцина доступна. Наиболее часто используемая зарегистрированная вакцина – это Combitex, российская вакцина, Engerix В – британская вакцина и Shanvac В – индийская вакцина. В соответствии с календарем прививок по эпидемиологическим показаниям вакцинируются дети и взрослые, члены семей, в которых имеются носители вируса гепатита В, дети домов ребенка, детских домов, интернатов, доноры крови, пациенты отделений гемодиализа и лица с онкогематологическими заболеваниями, лица, контактирующие с инфицированным материалом, студенты медицинских ВУЗов и средних медицинских учебных заведений. Все врачи должны быть вакцинированы. Ну, и, безусловно, наркоманы – наиболее сложная категория.
Вакцинация привела к очень существенным позитивным сдвигам. По официальным данным (данные профессора Шагильдяна И.В.), в 2000 году острый гепатит регистрировался у 42-43 человек на 100 тысяч населения в год, носителей инфекции регистрировалось около 100 человек на 100 тысяч населения в год. Это, можно сказать, было стартом вакцинации. К 2007 году число случаев острого гепатита В – я еще раз напоминаю, что это желтушная форма, то есть это не весь острый вирусный гепатит, а лишь часть его, но, тем не менее, снизилось с 43 до 5 на 100 тысяч населения в год. А число носителей уменьшилось более чем вдвое – до 42-43 на 100 тысяч населения в год.
Возникает вопрос: «Эти успехи должны нас успокаивать или они носят относительный характер?» Сравним Россию с Италией. Почему с Италией? Потому что Италия до недавнего времени рассматривалась и по существу относилась к странам с наиболее высокой заболеваемостью вирусными гепатитами, в том числе, и вирусным гепатитом В. Какие же цифры мы можем получить у нас в стране и сравнительные оценки ситуации с итальянцами? В начале 90-х годов заболеваемость в Италии составляла 3,4% – это близко к тому, что сейчас мы регистрируем в подавляющем большинстве регионов России. В настоящее время распространенность, то есть число больных хроническим гепатитом В и носителей в Италии составляет 1% – эта цифра, по существу, должна служить своеобразным путеводителем для нас. Заболеваемость острым гепатитом в Италии в 90-х годах составляла 5,1%, в настоящее время в России - 5,3%. Следовательно, мы с нашими достижениями находимся примерно на уровне 1990-х годов развития ситуации с гепатитом В в Италии. В настоящее время в Италии регистрируют 1,3 заболевших на 10 тысяч населения в год. Вакцинация в Италии была начата примерно на 10 лет раньше чем в России, и вакцинировались все новорожденные и подростки, а в настоящее время прививается до 94% населения страны. Вот это – своеобразный ориентир, к которому сейчас должна стремиться Россия. И при должной настойчивости, при большом охвате, по всей вероятности, мы сможем достичь достаточно хороших результатов.
Вместе с тем полезно проанализировать ситуацию, которая складывается с вирусным гепатитом В применительно к специализированным стационарам. В клинике пропедевтики внутренних болезней, гастроэнтерологии и гепатологии им. В.Х. Василенко была проанализирована структура пациентов с инфекцией вирусным гепатитом B в 2006, 2007, 2008 годах. Всего было проанализировано 7360 пациентов с гепатитом В с заболеваниями печени. Из них 8% оказались серопозитивными по маркерам вируса гепатита В и 92% – серонегативными. Среди 8% серопозитивных пациентов, что составляет 578 человек, 16% – это лица, которых можно рассматривать в качестве кандидатов для лечения, то есть это лица, у которых выявляется основной маркер – поверхностный антиген гепатита В – HBs-антиген. В абсолютных показателях эта цифра составила 92 человека (см. рис. 1).
Рис. 1. Структура HBV-инфекции

Таким образом, в общей структуре проанализированных пациентов, находившихся на стационарном лечении отделении гепатологии, из 7360 человек кандидатами для лечения оказались около 1% пациентов (см. рис. 2) – это лица с различными комбинациями маркеров вируса гепатита В. Эти комбинации отражают фазы естественного течения HBV-инфекции и, в соответствии с последними данными Европейского общества по изучения печени (EASL 2009) и Американского общества по изучению печени (AASLD 2009), выделяют пять фаз (см. рис. 3), из которых, по меньшей мере, две требуют облигатного лечения.
Рис. 2. Структура HBV-инфекции

Рис. 3. Естественное течение HBV-инфекции
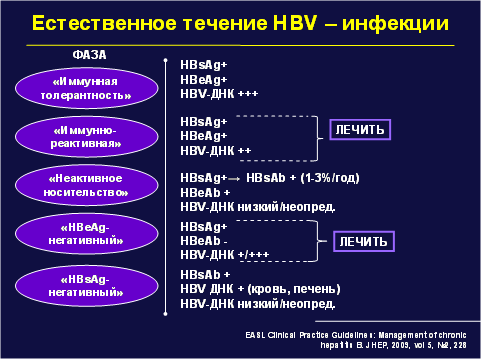
Первый вариант – это пациенты, находящиеся в так называемой иммунореактивной фазе. У них выявляется положительный маркер поверхностного антигена – HBs-антиген и ДНК вируса гепатита В. Второй вариант, требующий облигатного лечения – это HBе-антиген негативный. У таких пациентов мы определяем позитивный маркер вируса поверхностного антигена – HBs-антиген, отрицательный – HBе-антиген. Эта фаза носит также название «фазы реактивации». Вот это – две основных группы, которые в первую очередь требуют лечения ХГВ.
Среди пациентов, поступающих в стационар и приходящих на амбулаторный прием необходимо выявлять группы риска. В первую очередь, это пациенты с онкогематологическими заболеваниями по вполне понятной причине: большие, массивные переливания крови и кровезаменяющих препаратов и низкий уровень иммунной защиты; во-вторых – это ВИЧ-инфицированные; в-третьих – пациенты, которым осуществлялась трансплантация (костного мозга, печени, почки). И, наконец, группа пациентов, которые принимают следующие лекарственные препараты: иммуносупрессоры, или моноклональные антитела, химиотерапевтические препараты и комбинации, лечение Anti-CD20 (ритуксимаб), лечение Anti-CD52 (алемтузумаб) и, наконец, лечение ингибиторами фактора некроза опухоли (инфликсимаб). Помимо тех привычных угроз, которые стоят за хроническим инфицированием вирусом гепатита В, мы должны помнить, что с 1980-х годов, когда распространенность инфицирования вирусом гепатита В и вирусом гепатита С приобрела широкие масштабы, накапливается своеобразная критическая масса пациентов, которые длительное время или демонстрируют вполне определенную клинику хронического гепатита, или являются больными без четких клинических проявлений, и мы относим их к носителям инфекции. Вне зависимости от того, имеется ли яркая клиническая симптоматика или нет, само по себе носительство, инфицирование вирусом гепатита В – это уже огромный риск развития гепатоцеллюлярной карциномы. Следует отметить, что с каждым годом количество выявляемых пациентов с гепатоцеллюлярной карциномой, несмотря на относительное постоянство больных циррозом печени и больных вирусным циррозом печени, увеличивается, причем почти в линейной зависимости.
По данным заболеваемости и распространенности гепатита В в России носителями инфекции вируса гепатита В являются около 3 миллионов человек, кандидатами для лечения – примерно 750 тысяч. Получают же лечение по самым демократическим подсчетам 75 тысяч, то есть 10% от общего числа нуждающихся. Эта группа получает современное лечение интерферонами и аналогами нуклеоз(т)идов. В соответствии с международными рекомендациями для лечения вирусного гепатита B в России используются стандартные интерфероны, пегилированные интерфероны – альфа и аналоги нуклеоз(т)идов [2]. Конечно, наиболее удобным методом лечения пациентов с хроническим вирусным гепатитом В является применение аналогов нуклеоз(т)идов, так как согласно современным рекомендациям основной целью терапии ХГВ является стойкое подавление вирусной репликации и максимально долгое поддержание ее на неопределяемом уровне с целью профилактики развития осложнений ХГВ – цирроза печени и ГЦК. Очевидно, что для достижения этой цели в большей степени подходят аналоги нуклеозидов, чем интерфероны, как пероральные препараты с высоким профилем безопасности, и которые могут применяться длительно и непрерывно (в отличие от нуклеоз(т)идов, интерфероны имеют, помимо частых побочных эффектов, ограниченный срок терапии – 48 недель. Если в течение этого срока поставленные цели лечения не достигаются, дальнейшее использование препарата считается нецелесообразным с точки зрения непосредственного воздействия на вирус).
Применение простых и пегелированных интерферонов для лечения ХГВ ограничено развитием частых побочных эффектов (88% пациентов имеют выраженные побочные эффекты на терапии) и невысокой эффективностью - эффективность составляет не более 20-25%, особенно когда речь идет о терапии HbeAg- негативного хронического гепатита В, генотип Д (именно эта форма ХГВ преобладает на территории РФ) [3,4] . Кроме того, интерфероны противопоказаны при наличии цирроза и после трансплантации печени.
Из аналогов нуклеоз(т)идов у нас в стране зарегистрировано три препарата: Энтекавир (Бараклюд), Ламивудин (Зеффикс) и Телбивудин (Себиво). В краткосрочном плане (терапия на протяжении года) эффективность этих препаратов примерно одинакова. Однако, нужно понимать, что лечение хронического гепатита В требует длительного назначения противовирусных препаратов и здесь необходимо учитывать профиль резистентности аналогов нуклеоз(т)идов, так как различные препараты обладают различной величиной генетического барьера к развитию резистентности. Ламивудин обладает умеренной противовирусной активностью и наиболее низким генетическим барьером и вызывает развитие резистентности довольно быстро: уже ко второму году – 46% пациентов резистентны к лечению ламивудином, а к четвертому году – до 70% и более [5]. Телбивудин и энтекавир сопоставимы по эффективности противовирусного действия, но отличаются по частоте развития резистентности. Телбивудин, как и ламивудин, обладает низким генетическим барьером к развитию резистентности. В отношении телбивудина у нас нет результатов длительного его применения – мы оперируем данными эффективности и безопасности 2-х летней терапии телбивудином, полученными в рамках регистрационного исследования GLOBE. Частота развития устойчивых штаммов при лечении телбивудином пациентов, ранее не получавших аналоги нуклеозидов в течении 2 лет составляет 9 % у HbeAg- негативных больных и 22% у HbeAg-позитивных больных с ХГВ [6] (см. рис.4).
Рис. 4. Риск развития резистентности при лечении нуклеоз(т)идными аналогами пациентов, ранее не получавших аналогов нуклеоз(т)идов.
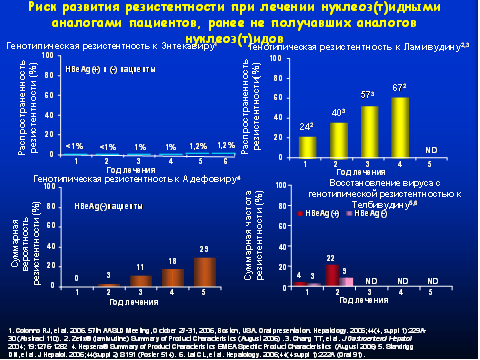
Учитывая наличие перекрестной резистентности телбивудина с ламивудином, в отличие от энтекавира телбивудин не применяется при лечении ламивудин-рефрактерных пациентов.
Очень важно отметить тот момент, что развитие резистентности к ламивудину и телбувудину в дальнейшем уменьшает возможности лечения пациентов, так как терапия этими препаратами способствует развитию резистентности и к другим аналогам нуклеоз(т)идов (перекрестная резистентность) [7].
Генотипическая резистентность к энтекивиру в течение 6-ти лет терапии у пациентов, ранее не получавших аналоги нуклеоз(т)идов, составляет 1,2% [8]. Таким образом, энтекавир, в отличие от телбивудина, демонстрирует наличие высокого генетического барьера к развитию резистентности у пациентов, ранее не получавших лечение нуклеоз(т)идами.
Как уже упоминалось ранее, основной задачей терапии ХГВ является профилактика прогрессирования заболевания и развития цирроза и гепатоцеллюлярной карциномы, что достигается путем мощного и стойкого подавления вирусной нагрузки до неопределяемого уровня. На сегодняшний день четко продемонстрировано, что именно вирусная нагрузка является основным и независимым прогностическим фактором, влияющим на развитие осложнений ХГВ. В свою очередь, отсутствие вируса ГВ способствует гистологическому улучшения картины печени и профилактике цирроза и гепатоцеллюлярной карциномы.
И на сегодняшний момент доступны данные длительного применения энтекавира, которые демонстрируют, что его длительное применение приводит к обратному развитию фиброза и способствует дальнейшему улучшению гистологических показателей у HBeAg (+) и HBeAg (-) пациентов с хроническим гепатитом В [9].
Теперь опять вернемся к структуре пациентов, которым показана терапия ХГВ. Итак, лишь 10% от общего количества нуждающихся получает современное лечение: интерфероны (классические и пегилированные) и аналоги нуклеоз(т)тидов. 90% пациентов получают так называемое альтернативное лечение. Так, наиболее изученными препаратами, не приносящими подавление вирусной инфекции, но, во всяком случае, снимающими в определенной степени некровоспалительную реакцию, являются Эссенциале, Силебинин, урсодезоксихолевая кислота, глицерризиновая кислота, и лечение некоторыми травами. Следовательно, пока что очень небольшая группа пациентов в России в состоянии получать адекватное рекомендованное международными гепатологическими ассоциациями лечение хронического гепатита В.
Когда такие пациенты доходят до стадии осложнений – цирроза печени, или у них обнаруживается на ранней стадии гепатоцеллюлярная карцинома, конечно, методом выбора является трансплантация печени. По данным статистики Московского городского центра трансплантации печени с 1999 года по 2008 год в общей структуре трансплантации печени пациенты, инфицированные вирусом гепатита В (вирусные циррозы В), а также комбинация вирусных циррозов В и гепатоцеллюлярная карцинома составляют 18% от общего количества лиц, которым осуществляется трансплантация печени. Конечно, этот метод лечения должен в России применяться гораздо шире – регионы должны обладать возможностью и иметь центры трансплантации печени.
Литература:
- Lok A.S., 23.03.2009, 13th International Symposium on viral hepatitis and liver diseases
- Papatheodoridis GV, Manolakopoulos S, Dusheiko G, Archimandritis AJ. Therapeutic strategies in the management of patients with chronic hepatitis B virus infection. Lancet Infect Dis. 2008 Mar;8(3):167-78.
- Lau GK, Piratvisuth T, Luo KX, Marcellin P, Thongsawat S, Cooksley G, Gane E, Fried MW, Chow WC, Paik SW, Chang WY, Berg T, Flisiak R, McCloud P, Pluck N; Peginterferon Alfa-2a HBeAg-Positive Chronic Hepatitis B Study Group.Peginterferon Alfa-2a, lamivudine, and the combination for HBeAg-positive chronic hepatitis B. N Engl J Med. 2005 Jun 30;352(26):2682-95.
- Marcellin P, Lau GK, Bonino F, Farci P, Hadziyannis S, Jin R, Lu ZM, Piratvisuth T, Germanidis G, Yurdaydin C, Diago M, Gurel S, Lai MY, Button P, Pluck N; Peginterferon Alfa-2a HBeAg-Negative Chronic Hepatitis B Study Group.Peginterferon alfa-2a alone, lamivudine alone, and the two in combination in patients with HBeAg-negative chronic hepatitis B. N Engl J Med. 2004 Sep 16;351(12):1206-17.
- EASL Clinical Practice Guidelines: management of chronic hepatitis B. European Association For The Study Of The Liver. J Hepatol. 2009 Feb;50(2):227-42.
- Liaw YF, Gane E, Leung N, Zeuzem S, Wang Y, Lai CL, Heathcote EJ, Manns M, Bzowej N, Niu J, Han SH, Hwang SG, Cakaloglu Y, Tong MJ, Papatheodoridis G, Chen Y, Brown NA, Albanis E, Galil K, Naoumov NV; GLOBE Study Group. 2-Year GLOBE trial results: telbivudine Is superior to lamivudine in patients with chronic hepatitis B. Gastroenterology. 2009 Feb;136(2):486-95.
- Locarnini S, et al. Antiviral Therapy 2004;9:145-48.
- Tenney, DJ M, et al 44th EASL, April 22–6, 2009, Copenhagen, Denmark. Oral 20. J. Hepatol 2009;50(suppl 1), S10.
- Liaw et al., Hepatology. 2008;48:(suppl.):706A (abstract 894)