26 июня 2000 года можно считать датой, перевернувшей представление ученых всего мира о строении человека, именно в этот день президент США Билл Клинтон и британский премьер-министр Тони Блэр объявили о завершении создания «черновика» генома. Этот грандиозный замысел по расшифровке генома человека (The Human Genome Project, HGP) являлся международным научно-исследовательским проектом, главной целью которого было определить последовательность нуклеотидов, которые составляют ДНК и идентифицировать 20—25 тысяч генов в человеческом геноме.
Трёхмиллиардный проект был формально запущен в 1990 году Министерством энергетики США и Национальным институтом Здравоохранения, и ожидалось, что он продлится 15 лет, однако, исследование было окончено досрочно, в апреле 2003 года, а в мае 2006 года, умы ученой общественности вновь всколыхнулись, когда в журнале Nature была опубликована последовательность последней хромосомы — хромосомы 1.
К тому времени фарминдустрия набирала все больше и больше оборотов, и если в 1993 году для одобрения нового лекарственного препарата требовалось 27 месяцев, в 2003 году, всего лишь 14. Но у каждой медали есть и оборотная сторона, которой в данном случае являлись нежелательные лекарственные реакции, число которых росло пропорционально регистрации новых препаратов.
Все вышесказанное привело к созданию революционной науки фармакогенетики, изучающей индивидуальные различия в ответ на лекарственные препараты, которые обусловлены аллельными вариациями в генах, определяющими метаболизм лекарства, его эффективность и токсичность.
Большое применение фармакогенетика нашла в кардиологии, что неудивительно учитывая тот факт, что пациентам, к примеру, перенесшим инфаркт миокарда (ИМ) врачи назначают одновременно 6-7 препаратов, которые могут вступать в лекарственные взаимодействия, ослабляя, или потенцируя, эффекты друг друга.
Основными ферментами, участвующими в метаболизме лекарств, являются: CYP2D6, CYP2C9 (включая VKORC1), CYP2C19, CYP3A4 и CYP3A5. Именно их генетические варианты определяют индивидуальную реакцию на назначение того или иного препарата. По данным последних исследований, около 85% популяции имеют один или более дефект в генах, кодирующих вышеперечисленные ферменты.[1]
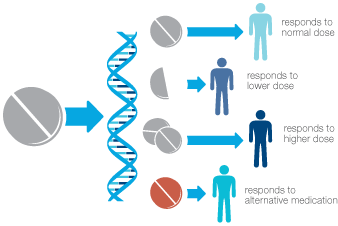
Всех индивидуумов можно разделить на 4 категории соответственно их способности метаболизировать лекарственные препараты:[5]
- Нормальные метаболизаторы (генотип включает в себя две активные формы гена, ответственные за «производство» метаболизирующего фермента и, следовательно, обладающий полной мощностью превращения лекарственного препарат). Таким лицам можно назначать препараты в стандартной дозе.
- Промежуточные метаболизаторы (генотип, согласующийся с данным фенотипом, содержит только одну активную форму гена, отвечающую за продукцию фермента, что служит причиной снижения способности метаболизировать лекарство). Данной группе индивидуумов требуется назначение дозы ниже средней для достижения оптимального терапевтического ответа.
- Медленные метаболизаторы (генотип не содержит активных форм гена, что приводит к «дефициту» лекарственного метаболизма). Индивидуумы, имеющие данный тип метаболизма, имеют повышенный риск развития лекарственно-индуцированных побочных эффектов или отсутствия терапевтического эффекта из-за невозможности генерировать активную форму препарата.
- Быстрые или ультрабыстрые метаболизаторы (генотип включает в себя три и более активных генов, следствием чего является увеличение метаболического потенциала). Лица, относящиеся к данной категории, нуждаются в назначении более высокой дозы препарата для достижения терапевтического ответа.
Если посмотреть на метаболизм часто назначаемых кардиологических препаратов, то за него отвечают следующие изоферменты:[2,3,4]
| Препарат | Изофермент | Препарат | Изофермент |
| клопидогрел | CYP2C19 | метопролол | CYP2D6 |
| варфарин | CYP2C9 и VKORC1 | изосорбид | NAT1;NAT2 |
| тикагрелор | CYP2C19 | карведилол | CYP2D6 |
Как видно из таблицы, большая часть препаратов метаболизируется при помощи цитохрома P450 (CYP), при этом по данным проведенных генетических популяционных исследований, значительная часть индивидуумов имеет вариабельность данной ферментной системы.[4]
| Ген | Медленные метаболизаторы | Промежуточные метаболизаторы | Нормальные метаболизаторы | Быстрые или ультрабыстрые метаболизаторы |
| CYP2D6 | 10% | 35% | 48% | 7% |
| CYP2C9 | 2-4% | >35% | ~60% | нет |
| CYP2C19* | 2-20% | 24-36% | 14-44% | 30% |
*зависит от этнической принадлежности
| Ген | Вариант активности | Кавказцы | Азиаты | Африканцы |
| CYP3A4 | уменьшение | 5,3% | 0% | 0% |
| CYP3A5 | уменьшение | 93% | 75% | 27-50 |
Возрастающий интерес ученых и самих пациентов к такому персонализированному подходу в выборе терапии, подстегивает индустриальные компании к созданию простых и приемлемых по цене тестов, однако, на настоящий момент, они еще не вошли в широкую практику и доступны не во всех странах мира.
Литература.
- FDA.gov [Internet]. Silver Spring, MD: U.S. Food and Drug Administration; c2007 [updated 2013 Apr 10; cited 2013 Sep 3].
- The International Warfarin Pharmacogenetics Consortium, Klein TE, Altman RB, Eriksson N, Gage BF, Kimmel SE et al. Estimation of the warfarin dose with clinical and pharmacogenetic data. N Engl J Med. 2009;360:753-64.
- Peyvandi F, Spreafico M, Siboni SM, Moia M, Mannucci PM. CYP2C9 genotypes and dose requirements during the induction phase of oral anticoagulation therapy. Clinical Pharmacology and Therapeutics. 2004 Mar; 75(3):198-203.
- Lee SJ, Usmani KA, Chanas B, Ghanayem B, Xi T, Hodgson E et al.: Genetic findings and functional studies of human CYP3A5 single nucleotide polymorphisms in different ethnic groups. Pharmacogenetics. 2003; 13(8):461-72.
- http://youscript.com.