Общественная Система
усовершенствования врачей
Пульмонология
Вейпинг, пагубная привычка может обернуться тяжелым поражением легких
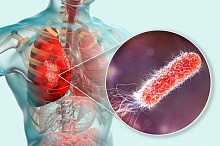
За июль 2019 года в Департаменте Здравоохранения Висконсин (США) были зарегистрированы 8 случаев тяжелых заболеваний легких среди подростков.
Польза и риски короткого курса антибиотиков при лечении пневмонии
Исследователи из США проанализировали предикторы и исходы, ассоциированные с длительной необоснованной антибиотикотерапией.
Поможет ли биологический препарат бенрализумаб снизить частоту обострений ХОБЛ?
Бенрализумаб (Фазенра®) - моноклональное антитело против рецептора интерлейкина-5.
Европа сказала фенспириду твердое нет
Европейское Медицинское Агентство (ЕМА) рекомендовало отозвать разрешение на продажу фенспирида в связи с сердечными рисками.
Повышен ли риск развития респираторных симптомов на фоне использования электронных сигарет?
Недавно мы рассказывали о негативных сердечно-сосудистых последствиях использования электронных сигарет. Пришло время поговорить о возможных последствиях для органов дыхания.
Почему не следует назначать антибиотики при обострениях бронхиальной астмы?
Американские исследователи оценили в ретроспективном исследовании исходы антибиотикотерапии у больных с обострением астмы.
Экстренное прекращение продажи препарата для лечения кашля фенспирида
Представительство АО «Лаборатории Сервье» (Франция) в Российской Федерации сообщает о решении Французского Национального Медицинского Агентства (ANSM) о приостановлении действия регистрационных удостоверений лекарственных препаратов, содержащих фенспирид, и об их изъятии из обращения.
Популярные бензодиазепины повышают риск развития пневмонии
В новом систематическим обзоре и мета-анализе исследователи оценили частоту развития пневмонии на фоне приема бензодиазепинов.
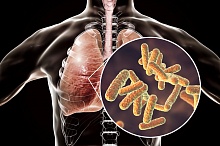
Оборотная сторона опиоидов внебольничная пневмония
Американские исследователи оценили связь между назначением опиоидов и внебольничной пневмонией у пациентов без и с ВИЧ-инфекцией.
Повышение риска неинфекционной пневмонии на фоне препарата устекинумаб
Американское US Food and Drug Administration (FDA) провело проверку безопасности биологического препарата устекинумаб (человеческое моноклональное антитело класса IgG1k против интерлейкинов 12 и 23).